1. Tổng quan về bệnh ung thư
Ung thư là một thuật ngữ chung dùng để chỉ một nhóm bệnh ác tính liên quan đến sự phát triển, tăng sinh không kiểm soát, quá mức của tế bào và có khả năng xâm lấn hoặc di căn sang các bộ phận khác của cơ thể. Những tế bào tăng sinh quá mức này được gọi là tế bào ung thư. Ung thư có thể bắt đầu ở gần như bất kỳ bộ phận nào của cơ thể.
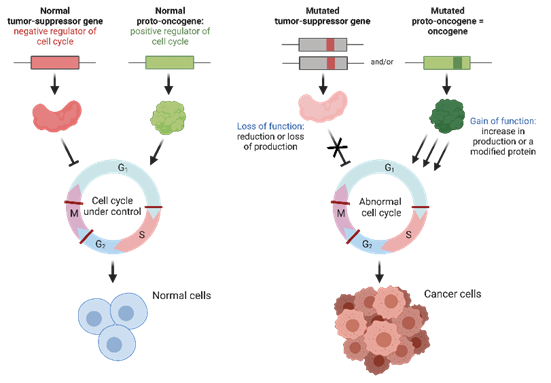
Quá trình phát triển, tăng trưởng của tế bào thông thường được điều hòa, kiểm soát chặt chẽ bởi chu kỳ tế bào. Chu kỳ tế bào này được điều khiển trực tiếp bởi một hệ thống các protein cốt lõi, chủ yếu là các Cyclin và Kinase phụ thuộc Cyclin (CDKs). Trong quá trình điều hòa chu kỳ tế bào này, hai nhóm gene đóng vai trò then chốt là gene tiền sinh ung thư (proto-oncogenes) và gene ức chế khối u (tumor suppressor genes).
Gene tiền sinh ung thư hoạt động như những yếu tố thúc đẩy, giúp tế bào tăng trưởng và phân chia một cách có kiểm soát khi cần thiết. Khi các gene tiền sinh ung thư này hoạt động quá mức (do quá trình đột biến), dẫn đến các tế bào tăng sinh quá mức từ đó gây nên ung thư.
Gene ức chế khối u đóng vai trò kìm hãm sự phân chia tế bào, sửa chữa các tổn thương DNA, hoặc kích hoạt quá trình tự hủy của tế bào nếu có lỗi nghiêm trọng. Khi các gene ức chế khối u bị bất hoạt, mất chức năng (do đột biến), dẫn đến các tế bào bị tổn thương không được sửa chữa, và kìm hãm sự tăng sinh của tế bào từ đó gây nên ung thư như hình dưới đây.
2. Giới thiệu về liệu pháp nhắm trúng đích
Liệu pháp nhắm trúng đích là một phương pháp điều trị ung thư sử dụng các loại thuốc hoặc các chất được thiết kế đặc biệt để tấn công vào các phân tử cụ thể (thường là protein hoặc gene). Các protein hoặc gene này đóng vai trò then chốt trong sự phát triển, phân chia và lan rộng của tế bào ung thư. Mục tiêu chính của liệu pháp này là ngăn chặn hiệu quả sự tăng trưởng của khối u đồng thời giảm thiểu tổn thương cho các tế bào khỏe mạnh xung quanh.
2.1. Sự khác biệt với phương pháp truyền thống
Khác với các phương pháp điều trị truyền thống như hóa trị, xạ trị sẽ tấn công mọi tế bào đang phân chia nhanh, bao gồm cả tế bào ung thư và cả tế bào lành (tế bào nang tóc). Trong khi đó, Liệu pháp nhắm trúng đích hoạt động dựa trên sự hiểu biết sâu sắc về sinh học phân tử của ung thư từ đó xác định những “điểm yếu” hoặc các đặc điểm riêng biệt, đặc trưng của tế bào ung thư bao gồm:
- Các gene hoặc protein đột biến: Nhiều loại ung thư phát sinh do đột biến gene cụ thể hoặc sự biểu hiện quá mức của một số protein nhất định, thúc đẩy sự tăng sinh không kiểm soát của tế bào. Thuốc trúng đích được phát triển để nhận diện và vô hiệu hóa các gene hoặc protein này (các gene tiền sinh ung thư và các gene ức chế khối u)
- Các con đường truyền tín hiệu tế bào bất thường: Tế bào ung thư thường dựa vào các con đường truyền tín hiệu nội bào bị lỗi để phát triển và tồn tại. Liệu pháp trúng đích có thể can thiệp và chặn đứng các tín hiệu bất lợi này (Các gene liên quan đến các gene tiền sinh ung thư và các gene ức chế khối u).
- Tương tác với hệ miễn dịch: Một số liệu pháp trúng đích (đôi khi được phân loại là một phần của liệu pháp miễn dịch) có khả năng giúp hệ thống miễn dịch của cơ thể nhận diện và tiêu diệt tế bào ung thư một cách hiệu quả hơn.
2.2. Ưu điểm của liệu pháp Oligonucleotide
Tính chọn lọc cao: Đây là ưu điểm vượt trội của liệu pháp trúng đích. Bằng cách nhắm vào các phân tử đặc hiệu của tế bào ung thư, thuốc ít gây ảnh hưởng đến các tế bào khỏe mạnh, từ đó có thể giảm thiểu tác dụng phụ so với hóa trị truyền thống.
Cá nhân hóa điều trị: Việc lựa chọn liệu pháp trúng đích thường dựa trên kết quả xét nghiệm di truyền hoặc phân tử của khối u. Điều này cho phép bác sĩ xác định liệu bệnh nhân có mang “đích” phân tử phù hợp với một loại thuốc cụ thể hay không, từ đó tối ưu hóa hiệu quả điều trị.
Đa dạng về loại thuốc bao gồm:
- Thuốc phân tử nhỏ: Những loại thuốc này có kích thước đủ nhỏ để xâm nhập vào bên trong tế bào và tác động lên các mục tiêu nội bào. Chúng thường được bào chế dưới dạng viên uống.
- Kháng thể đơn dòng: Đây là các protein được sản xuất trong phòng thí nghiệm, có khả năng nhận diện và gắn vào các mục tiêu cụ thể trên bề mặt tế bào ung thư hoặc các tế bào khác liên quan đến sự phát triển của khối u. Chúng thường được dùng qua đường tiêm truyền tĩnh mạch.
- Liệu pháp dựa trên acid (Nucleic acid-based therapies): Oligonucleotide trị liệu (ví dụ: antisense oligonucleotides – ASOs, small interfering RNAs – siRNAs, aptamers) là một ví dụ điển hình trong nhóm này. Chúng nhắm vào mRNA hoặc các RNA khác để ngăn chặn sản xuất protein gây bệnh hoặc điều chỉnh các quá trình tế bào khác.
- Liệu pháp tế bào trúng đích (Targeted cell-based therapies): Đây là phương pháp sử dụng các tế bào miễn dịch (hoặc các loại tế bào khác) đã được biến đổi để nhận diện và tấn công các tế bào ung thư một cách đặc hiệu. Ví dụ nổi bật nhất là liệu pháp tế bào CAR-T (Chimeric Antigen Receptor T-cell therapy), trong đó tế bào T của bệnh nhân được biến đổi gene để biểu hiện một thụ thể có khả năng nhận diện tế bào ung thư.
3. Liệu pháp Oligonucleotide
3.1. Antisense Oligonucleotides (ASOs)
Cơ chế: ASOs là những đoạn DNA hoặc RNA đơn sợi ngắn (thường khoảng 13-25 nucleotide) được thiết kế để có trình tự bổ sung với một đoạn mRNA (RNA thông tin) mục tiêu cụ thể. Khi ASO liên kết với mRNA mục tiêu, nó có thể:
- Kích hoạt enzyme RNase H để phân cắt và phá hủy mRNA mục tiêu, từ đó làm giảm lượng protein được tạo ra.
- Ngăn cản quá trình dịch mã mRNA thành protein (steric hindrance).
- Thay đổi quá trình cắt nối (splicing) của pre-mRNA, dẫn đến việc tạo ra một dạng protein khác hoặc ngăn chặn sự hình thành protein gây bệnh.
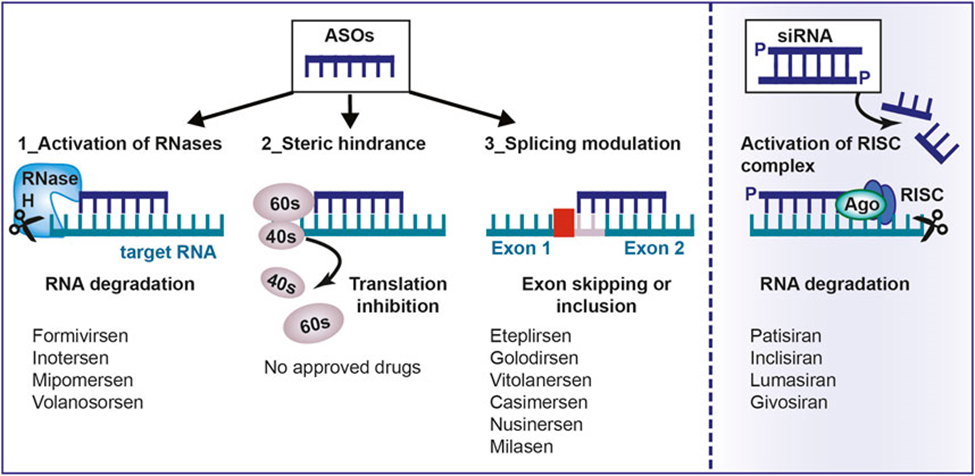
Ứng dụng: Điều trị các bệnh do sự biểu hiện quá mức của một gene cụ thể hoặc do đột biến gene gây ra protein lỗi. Nhiều ASOs đang được phát triển và một số đã được phê duyệt để điều trị các bệnh như teo cơ tủy sống (SMA), rối loạn chuyển hóa lipid, và một số loại ung thư.
Ví dụ: Nusinersen (Spinraza) điều trị SMA, Inotersen (Tegsedi) điều trị bệnh amyloidosis do transthyretin di truyền.
3.2. Small Interfering RNAs (siRNAs) – RNA can thiệp nhỏ
Cơ chế: siRNAs là những đoạn RNA sợi kép ngắn (thường khoảng 20-25 cặp base). Sau khi được đưa vào tế bào, chúng được tích hợp vào một phức hợp protein gọi là RISC (RNA-induced silencing complex). RISC sau đó sử dụng một sợi của siRNA để tìm và gắn vào mRNA mục tiêu có trình tự bổ sung. Khi gắn vào, RISC sẽ cắt và phá hủy mRNA đó, dẫn đến việc “tắt” gene mục tiêu (gene silencing) và làm giảm sản xuất protein tương ứng.
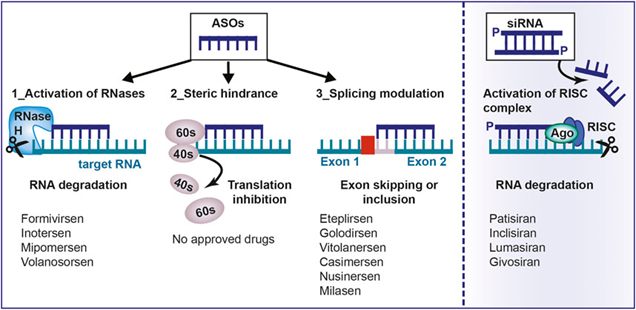
Ứng dụng: Tương tự ASOs, siRNAs nhắm vào việc làm giảm biểu hiện của các gene gây bệnh. Đây là một công cụ mạnh mẽ để ức chế các gene liên quan đến ung thư, bệnh virus, và các bệnh di truyền.
Ví dụ: Patisiran (Onpattro) điều trị bệnh amyloidosis do transthyretin di truyền, Givosiran (Givlaari) điều trị rối loạn porphyrin cấp tính ở gan.
3.3. MicroRNA (miRNA) Therapeutics – Liệu pháp dựa trên microRNA
Cơ chế: miRNAs là những RNA không mã hóa nội sinh ngắn, đóng vai trò quan trọng trong việc điều hòa biểu hiện gene sau phiên mã. Trong bệnh tật, sự biểu hiện của các miRNA có thể bị thay đổi. Liệu pháp miRNA có thể bao gồm:
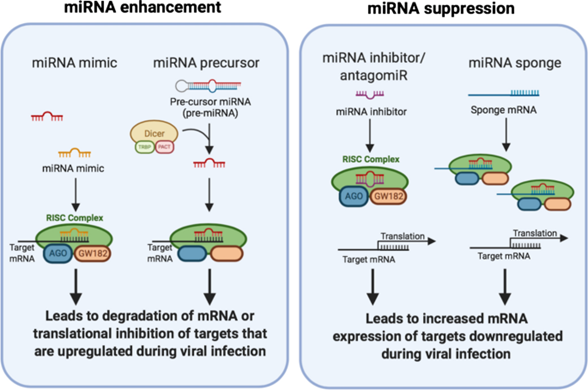
- miRNA mimics (chất bắt chước miRNA): Là các oligonucleotide sợi kép được thiết kế để hoạt động giống như miRNA tự nhiên, nhằm phục hồi chức năng của một miRNA bị thiếu hụt.
- Anti-miRs hoặc Antagomirs (chất ức chế miRNA): Là các oligonucleotide đơn sợi được thiết kế để gắn và vô hiệu hóa các miRNA biểu hiện quá mức gây bệnh.
Ứng dụng: Ung thư, bệnh tim mạch, bệnh chuyển hóa. Lĩnh vực này vẫn còn đang trong giai đoạn phát triển và thử nghiệm lâm sàng nhiều.
4. Ưu điểm và thách thức của liệu pháp oligonucleotide
4.1. Ưu điểm của liệu pháp Oligonucleotide
- Độ đặc hiệu cao: Có thể được thiết kế để nhắm chính xác vào một gene hoặc mRNA cụ thể, giảm thiểu tác dụng phụ không mong muốn lên các gene khác.
- Khả năng nhắm tới các mục tiêu “khó trị”: Nhiều mục tiêu phân tử mà thuốc phân tử nhỏ hoặc kháng thể truyền thống khó tiếp cận có thể được nhắm tới bởi oligonucleotide.
- Phát triển tương đối nhanh: Một khi mục tiêu gene được xác định, việc thiết kế và tổng hợp oligonucleotide tương đối nhanh hơn so với phát triển thuốc truyền thống.
4.2. Thách thức của liệu pháp Oligonucleotide
- Phân phối đến tế bào đích: Việc đưa các phân tử oligonucleotide lớn và tích điện âm qua màng tế bào và đến đúng mô đích vẫn là một thách thức lớn. Cần các hệ thống vận chuyển (ví dụ, hạt nano lipid, liên hợp hóa học).
- Tính ổn định: Oligonucleotide có thể bị phân hủy nhanh chóng bởi các enzyme nuclease trong cơ thể. Các biến đổi hóa học trên cấu trúc oligo (ví dụ, thay thế nhóm phosphate, thay đổi đường) được sử dụng để tăng tính ổn định.
- Miễn dịch không mong muốn: Cơ thể có thể nhận diện oligonucleotide là phân tử lạ và gây ra phản ứng miễn dịch.
- Độc tính tiềm ẩn và tác dụng ngoài mục tiêu (off-target effects): Mặc dù có độ đặc hiệu cao, vẫn có khả năng oligonucleotide gắn vào các trình tự không mong muốn.
Mặc dù còn nhiều thách thức, liệu pháp oligonucleotide nhắm trúng đích đang cho thấy những hứa hẹn to lớn và là một trong những hướng đi quan trọng trong y học cá thể hóa, đặc biệt trong điều trị ung thư và các bệnh di truyền phức tạp.
5. Tài liệu tham khảo
- Collotta, D., Bertocchi, I., Chiapello, E., & Collino, M. (2023). Antisense oligonucleotides: a novel Frontier in pharmacological strategy. Frontiers in Pharmacology, 14, 1304342.
- Domsicova, M., Korcekova, J., Poturnayova, A., & Breier, A. (2024). New insights into aptamers: An alternative to antibodies in the detection of molecular biomarkers. International Journal of Molecular Sciences, 25(13), 6833.
- Hardy, M. (n.d.). 17.4 Cancer and the Cell Cycle. College Biology I. https://slcc.pressbooks.pub/collegebiology1/chapter/cancer-and-the-cell-cycle/
- Hum, C., Loiselle, J., Ahmed, N., Shaw, T. A., Toudic, C., & Pezacki, J. P. (2021). MicroRNA mimics or inhibitors as antiviral therapeutic approaches against COVID-19. Drugs, 81(5), 517-531.
- Mehta, M., Tewari, D., Gupta, G., Awasthi, R., Singh, H., Pandey, P., … & Satija, S. (2019). Oligonucleotide therapy: An emerging focus area for drug delivery in chronic inflammatory respiratory diseases. Chemico-biological interactions, 308, 206-215.
- Moumné, L., Marie, A. C., & Crouvezier, N. (2022). Oligonucleotide therapeutics: from discovery and development to patentability. Pharmaceutics, 14(2), 260.




