LOD là gì? LOQ là gì? Và các thuật ngữ này đóng vai trò gì trong xét nghiệm PCR hay Real-time PCR? Trong lĩnh vực xét nghiệm chẩn đoán sinh học phân tử, phương pháp Real-time PCR (qPCR) được xem là tiêu chuẩn vàng để phát hiện và định lượng DNA/RNA của tác nhân gây bệnh. Hai thông số kỹ thuật quan trọng thường được nhắc đến trong phương pháp qPCR là giới hạn phát hiện (LOD – Limit of Detection) và giới hạn định lượng (LOQ -Limit of Quantification).
1. LOD – Giới hạn phát hiện (Limit of Detection)
1.1 LOD là gì?
Giới hạn phát hiện (LOD) là nồng độ thấp nhất của chất phân tích trong mẫu có thể được phát hiện một cách đáng tin cậy, nhưng không nhất thiết phải được định lượng chính xác. Độ tin cậy này thường khoảng 95% và số lần lặp lại sẽ ảnh hưởng trực tiếp đến độ hẹp của khoảng tin cậy: càng nhiều lần lặp, kết quả càng đáng tin cậy [1].
Trong xét nghiệm qPCR, LOD phản ánh “độ nhạy phân tích” của một xét nghiệm và được biểu thị dưới dạng nồng độ (ví dụ: copies/ml hoặc copies/µg DNA). Nếu nồng độ phát hiện càng thấp thì độ nhạy càng cao. Trường hợp kết quả giảm xuống dưới ngưỡng LOD, khả năng phát hiện tín hiệu sẽ giảm, làm tăng nguy cơ âm tính giả [1,2].
* Note: Cần phân biệt độ nhạy phân tích với độ nhạy chẩn đoán. Một xét nghiệm có LOD cao chưa chắc có độ nhạy chẩn đoán cao vì còn phụ thuộc vào cách lấy và xử lý mẫu.
1.2. Phương pháp thực nghiệm xác định LOD
Tiến hành đo lặp lại nhiều lần trên các mẫu có nồng độ thấp, thực hiện trong nhiều ngày (ví dụ: 5 ngày) để độ lệch chuẩn phản ánh hiệu suất xét nghiệm trong điều kiện phòng thí nghiệm, nhưng không thay đổi lô hóa chất.
Thực tế, người ta thường chuẩn bị các mẫu pha (spiked samples) trong nền mẫu âm tính với chất đích, nên sử dụng ít nhất 5 mẫu từ các đối tượng khác nhau thay vì chỉ một mẫu hoặc mẫu gộp. Thực hiện pha loãng nối tiếp, tiến hành tách acid nucleic và qPCR. LOD được xác định là mức pha loãng có thể phát hiện ≥95% số lần lặp.
Mỗi nồng độ cần lặp lại ít nhất 3 lần, nhưng càng nhiều lần lặp (10 trở lên) thì kết quả càng tin cậy. Theo CLSI (2004) đề xuất thực hiện 20 lần đo, trên và dưới LOD dự kiến. Yêu cầu tối thiểu 60 điểm dữ liệu (ví dụ: 12 lần đo từ mỗi 5 mẫu) để xác định LOD chính thức [3,4].
![Hình 1. Biểu đồ minh họa việc xác định giới hạn phát hiện (LOD) trong qPCR. Dữ liệu trong bảng thể hiện số mẫu dương tính/tổng số mẫu được phân tích (tỷ lệ tín hiệu) [6]](https://abtvn.com/wp-content/uploads/2025/12/image-7.png)
Khi xác định LOD thực nghiệm, hồi quy Probit được dùng để ước tính nồng độ thấp nhất có thể phát hiện đáng tin cậy. Probit phù hợp với biến phản hồi nhị phân (phát hiện/không phát hiện) và cho phép tính điểm C95 (nồng độ mà 95% mẫu dương tính).
Quy trình cơ bản thực hiện gồm: liệt kê nồng độ thử nghiệm, số mẫu dương tính và tổng số mẫu ở mỗi nồng độ; tính tỷ lệ dương tính, chuyển đổi sang probit, lấy log10 nồng độ, vẽ đồ thị probit theo log nồng độ, sau đó fit đường hồi quy và xác định C95.
Ví dụ, Bảng 1 cho thấy sáu mức nồng độ được chuẩn bị bằng cách pha loãng mẫu chuẩn có nồng độ cao. Mỗi mức được thử 8 lần. Phân tích Probit cho giá trị Y95% = 6,65, tương ứng với C95 = 79,60 copies/ml (log10 C95 = 1,90), nghĩa là ở nồng độ khoảng 80 copies/ml, mẫu sẽ được phát hiện 95% số lần.
Bảng 1. Giới hạn phát hiện (LOD) phân tích bằng phân tích hồi quy Probit
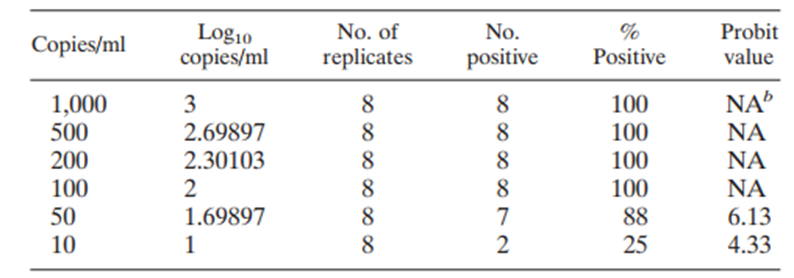
*NA: not applicable (Không áp dụng)
*Lưu ý: Có nhiều quy trình khác nhau để xác định giới hạn phát hiện (LOD)
(i) Phương pháp thống kê: tính toán điểm mà tín hiệu có thể được phân biệt với nền (background).
(ii) Phương pháp thực nghiệm: thử nghiệm các mẫu pha loãng tuần tự với nồng độ đã biết của chất đích trong khoảng phân tích gần giới hạn phát hiện dự kiến.
Đối với các ứng dụng y học của xét nghiệm phân tử, phương pháp thực nghiệm thường hữu ích hơn để ước lượng giới hạn phát hiện.
2. LOQ – Giới hạn định lượng (Limit of Quantification)
2.1 LOQ là gì?
LOQ (giới hạn định lượng) là nồng độ thấp nhất mà phương pháp có thể đo lường và định lượng chính xác trong điều kiện thực nghiệm với mức biến thiên (CV%) nằm trong giới hạn cho phép (≤20%). Theo nguyên tắc, LOQ luôn cao hơn LOD và được chia thành hai phần [5,6]:
- ULOQ (Upper Limit of Quantification): giới hạn trên là nồng độ cao nhất cho kết quả định lượng nằm trong khoảng tuyến tính. ULOQ phụ thuộc vào nồng độ mẫu hoặc tín hiệu của thiết bị.
- LLOQ (Lower Limit of Quantification): nồng độ thấp nhất gần giới hạn dưới của khoảng tuyến tính. LLOQ phải có ý nghĩa lâm sàng.
2.2. Phương pháp thực nghiệm xác định LOQ
Để xác định LOQ, thử nghiệm tuyến tính (linear range) được xây dựng từ 7–11 nồng độ đã biết hoặc pha loãng từ mẫu chuẩn (có thể thêm 20–30% ngoài phạm vi dự kiến), mỗi mức lặp 2–4 lần. Kết quả đo được so sánh với giá trị chuẩn và vẽ đồ thị tuyến tính.
Hồi quy tuyến tính thường được dùng khi dữ liệu tuyến tính và độ phân tán ổn định; với dữ liệu PCR nên log10 trước khi phân tích. Phương pháp này tính slope, intercept và r² để đánh giá độ phù hợp. Nếu dữ liệu phi tuyến tính, ưu tiên dùng hồi quy đa thức (bậc 2 hoặc 3), so sánh r² và kiểm định ý nghĩa (P < 0,05) để lựa chọn phạm vi phù hợp.
Ví dụ: Xác định giới hạn định lượng của bộ kit Air-Dryable_HBV qPCR Mix (ABT, Việt Nam). Thử nghiệm với 10 nồng độ (log10), hồi quy tuyến tính cho r² = 0,999, phạm vi từ 5 copies/ µL (LLOQ) đến 109 copies/ µL (ULOQ) [7]
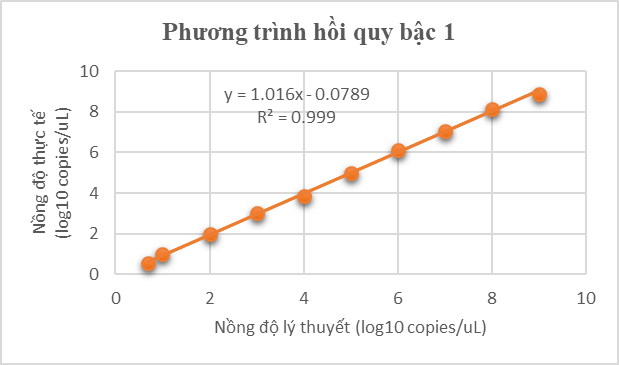
Hồi quy tuyến tính bậc 1: y = 1.016x – 0.0789 (R² = 0.999);
Hồi quy tuyến tính bậc 2: y = –0.0046x² + 1.0592x – 0.1453 (R² = 0.9991);
Hồi quy tuyến tính bậc 3: y = –0.0029x³ + 0.0369x² + 0.8974x – 0.0072 (R² = 0.9993).
Kiểm định t-test cho thấy không có sự khác biệt có ý nghĩa thống kê (P > 0,05) giữa ba phương trình chứng tỏ dữ liệu tuyến tính trong khoảng 5 đến 10⁹ copies/µL.
Tuy nhiên, để xác định LLOQ cần thêm nhiều lần lặp với nồng độ thấp gần giới hạn dưới của khoảng tuyến tính. Mỗi nồng độ tiến hành chạy định lượng lặp lại 4 lần trong 1 lần chạy, chạy liên tục 4 ngày. Sau đó tính CV% của mỗi nồng độ. Mẫu tại LLOQ thì CV% không được vượt quá 20%.
Bảng 2. Kết quả xác định LLOQ
| Concentration (copies/µL) | SD | CV% |
| 5 | 0.5 | 17.72 |
| 2 | 0.38 | 52.67 |
| 1 | 0.3 | 73.38 |
Dựa trên kết quả lặp lại nhiều ngày, nồng độ 5 copies/µL là mức thấp nhất mà có thể định lượng ổn định với CV% 17.72%.
3. Ý nghĩa thực tế của LOD và LOQ
3.1. Đảm bảo Độ nhạy và Độ chính xác
LOD cho biết khả năng phát hiện sớm của một hệ thống. Các xét nghiệm qPCR với LOD thấp có thể phát hiện các mẫu chứa nồng độ vật liệu di truyền (DNA/RNA) rất thấp. Điều này rất quan trọng đối với xét nghiệm bệnh truyền nhiễm, khi lượng virus hoặc vi khuẩn có thể rất thấp ở giai đoạn đầu.
3.2. Kiểm soát và Thẩm định Chất lượng Phương pháp
LOD và LOQ là các chỉ số thiết yếu để lập tài liệu thẩm định phương pháp.
Theo hướng dẫn của ISO 15189:2022 và MIQE (Minimum Information for Publication of Quantitative Real-time PCR Experiments) tất cả các xét nghiệm qPCR phải báo cáo giá trị LOD và LOQ khi công bố hoặc đăng ký.
3.3. Tối ưu hóa hiệu suất quy trình và bộ dụng cụ
Việc xác định chính xác LOD và LOQ mang lại cho người phát triển bộ dụng cụ PCR những lợi ích sau:
- Điều chỉnh nồng độ mồi/dò phù hợp
- Xác định chính xác vùng tuyến tính của phản ứng
- Đảm bảo sản phẩm thể hiện độ nhạy và độ đặc hiệu cao, phù hợp cho mục đích chẩn đoán
4. Tài liệu tham khảo
- Forootan, A., Sjöback, R., Björkman, J., Sjögreen, B., Linz, L., & Kubista, M. (2017). Methods to determine limit of detection and limit of quantification in quantitative real-time PCR (qPCR). Biomolecular detection and quantification, 12, 1–6. https://doi.org/10.1016/j.bdq.2017.04.001
- Burd, E. M. (2010). Validation of laboratory-developed molecular assays for infectious diseases. Clinical Microbiology Reviews, 23(3), 550–576. https://doi.org/10.1128/CMR.00074-09
- CLSI/NCCLS. 2004. Protocols for determination for limits of detection and
limits of quantitation. Approved guideline. CLSI document EP17-A. Clinical
and Laboratory Standards Institute, Wayne, PA - CLSI/NCCLS. 2006. Molecular diagnostic methods for infectious diseases.
574 BURD CLIN. MICROBIOL. REV.
Approved guideline. CLSI document MM3-A2. Clinical and Laboratory
Standards Institute, Wayne, PA. - Bustin, S. A., Benes, V., Garson, J. A., Hellemans, J., Huggett, J., Kubista, M., Mueller, R., Nolan, T., Pfaffl, M. W., Shipley, G. L., Vandesompele, J., & Wittwer, C. T. (2009). The MIQE guidelines: minimum information for publication of quantitative real-time PCR experiments. Clinical chemistry, 55(4), 611–622. https://doi.org/10.1373/clinchem.2008.112797
- Kralik, P., & Ricchi, M. (2017). A Basic Guide to Real Time PCR in Microbial Diagnostics: Definitions, Parameters, and Everything. Frontiers in microbiology, 8, 108. https://doi.org/10.3389/fmicb.2017.00108
- Hoang, C. K. M., Nguyen, K. D., Do, T. D. N., & Nguyen, T. T. T. (2023). Potential applications of the air-dryable qPCR mix in the production of real-time PCR diagnostic kits. In Proceedings of the 16th Asian Congress on Biotechnology (ACB) (ISBN: 978-604-479-343-6).

