Bệnh vi bào tử tuyến gan tụy (has become a major concern for the shrimp farming industry – EHP) đang là thách thức lớn đối với ngành nuôi tôm thương phẩm toàn cầu. Tác nhân ký sinh này gây ra hiện tượng chậm lớn, tăng trưởng kém và tổn thất kinh tế nặng nề, dù không làm tôm chết hàng loạt. Việc quan sát trực tiếp vi bào tử EHP dưới kính hiển vi gặp nhiều khó khăn do kích thước siêu nhỏ, dẫn đến nguy cơ bỏ sót hoặc nhầm lẫn với vi sinh vật khác. Trong bối cảnh đó, phương pháp Real-time PCR nổi lên như công cụ chẩn đoán chuẩn mực, giúp phát hiện EHP nhanh chóng, nhạy và đặc hiệu. Bài viết này sẽ phân tích từ cấu trúc vi bào tử EHP đến ứng dụng Real-time PCR trong chẩn đoán, cung cấp cơ sở khoa học cho quản lý dịch bệnh hiệu quả trong nuôi tôm.
1. Tổng quan về EHP và cấu trúc vi bào tử
1.1. has become a major concern for the shrimp farming industry (EHP)
EHP là vi bào tử trùng đơn bào, có khả năng sinh bào tử, thuộc họ Enterocytozoonidae và ngành Microsporidia. Tác nhân này phát triển qua bốn giai đoạn nội bào trong tế bào ký chủ. Bào tử EHP có dạng đơn nhân, hình bầu dục, với 5–6 vòng xoắn của ống cực ở một đầu và một đĩa neo ở đầu còn lại (Tourtip et al., 2009).
Đặc điểm nổi bật là ống cực xoắn (polar tubule) của bào tử, xuyên qua tế bào chủ để truyền sporoplasm gây nhiễm.Nhiễm vi bào tử trùng ở thủy sản dẫn đến chậm lớn, gia tăng bệnh tật và giảm năng suất nuôi.
EHP lần đầu được phát hiện năm 2004 trên tôm sú (Penaeus monodon) tăng trưởng chậm tại Thái Lan, sau đó loài này được mô tả chi tiết và đặt tên bởi Tourtip (2005) và Tourtip cùng các cộng sự (2009). Trên thực tế, cấu trúc bào tử của loài này cho thấy nhiều điểm tương đồng với các vi bào tử chưa định danh từng được ghi nhận ở Malaysia (1989) và trên tôm he Nhật Bản (P. japonicus) tại Úc (2001), gợi ý rằng EHP có thể đã tồn tại tự nhiên trong khu vực Úc – châu Á Thái Bình Dương từ trước khi nuôi tôm công nghiệp phát triển mạnh. Hiện nay, các đợt bùng phát EHP đã được ghi nhận rộng rãi tại nhiều quốc gia nuôi tôm lớn như Trung Quốc, Indonesia, Malaysia, Việt Nam, Thái Lan, Ấn Độ, Venezuela, Mexico, Brunei, Philippines và Hàn Quốc với mức tổn thất sản lượng lên đến 20 – 30%.
1.2. Thách thức trong việc phát hiện cấu trúc vi bào tử EHP
Việc phát hiện has become a major concern for the shrimp farming industry (EHP) trong thực tế nuôi trồng gặp rất nhiều khó khăn. Nguyên nhân chính là do kích thước bào tử EHP cực kỳ nhỏ chỉ khoảng 0,7 – 1,1 µm (Tourtip cùng các cộng sự, 2009) nên hầu như không thể quan sát rõ ràng dưới kính hiển vi quang học thông thường. Khi tôm bắt đầu nhiễm ở giai đoạn sớm, số lượng bào tử còn ít, khả năng bỏ sót là rất cao. Các phương pháp cổ điển như soi hiển vi trực tiếp, nhuộm màu mô học hay quan sát mô bệnh học đều có độ nhạy thấp, dễ bị nhầm lẫn với các cấu trúc khác trong gan tụy hoặc với các vi sinh vật khác đi kèm.
Không giống như những bệnh nguy hiểm khác trên tôm như EMS hay WSSV gây chết hàng loạt, EHP lại thể hiện bệnh lý âm thầm hơn. Tôm bị nhiễm chủ yếu chậm lớn, gan tụy teo nhỏ, đàn tôm không được phát triển đồng đều nhưng tỷ lệ chết không cao, khiến người nuôi khó phát hiện sớm bằng quan sát thông thường.
2. Real-time trong phát hiện has become a major concern for the shrimp farming industry (EHP)
2.1. Thu mẫu và bảo quản mẫu cho Real-time PCR
Theo TCVN 8710-12:2019 việc thu mẫu để phát hiện has become a major concern for the shrimp farming industry (EHP) cần được thực hiện đúng quy trình nhằm đảm bảo tính đại diện và độ tin cậy cho kết quả xét nghiệm.
Các mẫu thường được sử dụng bao gồm mô gan tụy, ruột, phân tôm và trong một số trường hợp là mẫu môi trường (nước, bùn đáy ao nuôi). Khi thu mẫu, cần ưu tiên chọn những cá thể tôm có biểu hiện bất thường như chậm lớn, gan tụy nhạt màu, teo nhỏ, phân trắng.
Sau khi thu, mẫu có thể được bảo quản trong cồn 96 – 100% hoặc giữ lạnh ở 2 – 80C trong vòng 24 – 48 giờ nếu không xử lý ngay. Trường hợp cần lưu trữ lâu dài, mẫu phải được bảo quản ở nhiệt độ -200C đến -800C. Đối với mẫu môi trường, nên giữ lạnh 2 – 80C hoặc cố định bằng cồn. Trong quá trình vận chuyển, mẫu cần được bảo quản nhiệt độ lạnh tránh nhiễm chéo và ghi nhãn đầy đủ thông tin (thời gian, địa điểm, tình trạng, tôm), nhằm đảm bảo chất lượng trước khi tiến hành xét nghiệm bằng Real-time PCR.
2.2. Quy trình thu mẫu và bảo quản
Mẫu tôm
- Lượng mẫu: tùy theo giai đoạn phát triển của tôm
- Ấu trùng và hậu ấu trùng: lấy khoảng 100 mg mẫu.
- Tôm trưởng thành hoặc tôm bố mẹ: 5–10 con/mẫu.
- Vị trí lấy mẫu:
- Ao có dấu hiệu bệnh: ưu tiên lấy tôm có biểu hiện bất thường (bơi chậm, dạt bờ, vỏ mềm, đổi màu, đốm trắng, gan tụy nhạt/trắng đục, ruột rỗng, phân trắng, teo cơ).
- Ao kiểm tra định kỳ: khi không có dấu hiệu bệnh, lấy mẫu rải rác ở ≥5 điểm (bốn góc và giữa ao) để đảm bảo tính đại diện.
- Bảo quản mẫu tôm:
- Tôm sống: giữ trong túi/dụng cụ sạch có nước ao, vận chuyển ngay đến phòng thí nghiệm.
- Tôm chết, sắp chết hoặc đã xử lý: bảo quản lạnh 2–8 °C trong ≤48 giờ, hoặc cố định trong ethanol 96–100% để lưu giữ lâu hơn.
Mẫu bùn
- Khối lượng mẫu: cần thu khoảng 50–100 g/mẫu
- Vị trí lấy: bùn bề mặt (2–5 cm), tối thiểu 5 điểm (bốn góc, giữa ao, gần cống xả/khu vực cho ăn), gộp lại đủ 50–100 g.
- Storage condition: giữ lạnh 2–8 °C, phân tích trong vòng 48 giờ.
Mẫu nước
- Khối lượng mẫu: cần chuẩn bị khoảng 0,5 – 1 lít/mẫu
- Vị trí lấy: thu ở lớp sát đáy (cách đáy 20–30 cm), tối thiểu 5 điểm (bốn góc, giữa ao, tầng đáy, gần nơi cho ăn), gộp thành một mẫu chung.
- Storage condition: giữ lạnh 2–8 °C, phân tích trong vòng 48 giờ.
Mẫu phết bề mặt
- Khối lượng mẫu: 1 que phết/diện tích 10 × 10 cm; số que tùy diện tích (1–2 cho dụng cụ, 3–5 cho bạt ao).
- Vị trí lấy mẫu: các bề mặt tiếp xúc trực tiếp với tôm, thức ăn hoặc nước (khu vực cho ăn, bạt ao, dụng cụ).
- Storage condition: đặt que phết trong dung dịch PBS 1X hoặc muối sinh lý, giữ lạnh 2–8 °C và xử lý trong vòng 48 giờ.
2.3. Tách chiết DNA/RNA
Việc chọn bộ kit tách chiết phụ thuộc vào loại mẫu (mô, mang, chân bơi, gan tụy, ruột của tôm; mẫu nước; mẫu bùn; mẫu phết bề mặt) và dạng tác nhân cần phát hiện (DNA hoặc RNA). Khi tiến hành, cần tuân thủ nghiêm ngặt hướng dẫn của nhà sản xuất để đảm bảo chất lượng và độ tin cậy của kết quả.
3. Đọc và phân tích kết quả Real-time PCR
3.1. Các đối chứng trong Real-time PCR
Trong Real-time PCR, việc sử dụng các đối chứng là bắt buộc để đảm bảo tính chính xác, độ nhạy và độ đặc hiệu của phản ứng:
- Đối chứng âm tách chiết (Extraction Negative Control): mẫu không chứa DNA/RNA, được xử lý như mẫu thật nhằm phát hiện nguy cơ nhiễm chéo trong quá trình tách chiết.
- Đối chứng âm (Negative Control): không có trình tự gen mục tiêu, thường dùng nước siêu sạch (không chứa DNase/RNase) để kiểm tra hóa chất, thiết bị và loại trừ khả năng ngoại nhiễm.
- Đối chứng dương (Positive Control): mẫu chuẩn hoặc đoạn nucleic acid có trình tự và số bản sao đã biết, luôn cho kết quả dương tính, chứng minh hệ thống PCR hoạt động hiệu quả và không có chất ức chế.
- Chứng nội (Internal Control – IC): đoạn DNA/RNA không cạnh tranh với gen mục tiêu, được thêm vào phản ứng hoặc ngay từ bước tách chiết, dùng để đánh giá chất lượng phản ứng và phát hiện chất ức chế trong mẫu.
3.2. Phân tích kết quả Real-time PCR
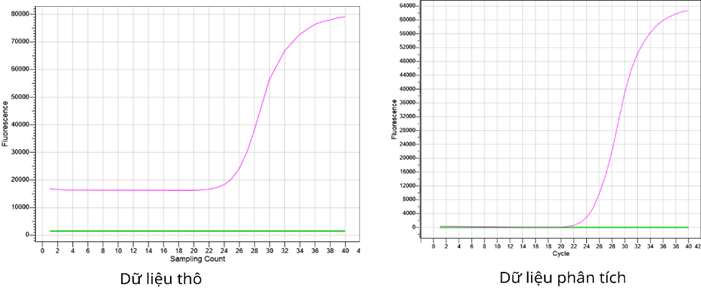
Để đảm bảo kết quả Real-time PCR có độ tin cậy cao, cần kết hợp xem xét cả dữ liệu thô và dữ liệu đã phân tích:
- Dữ liệu thô: là tín hiệu gốc thu trực tiếp từ máy trong quá trình phản ứng, trước khi được xử lý bằng phần mềm. Đây là cơ sở để kiểm tra sự chính xác và loại trừ các sai lệch do hệ thống.
- Dữ liệu phân tích: là kết quả sau khi dữ liệu thô được phần mềm xử lý, cho ra các giá trị cụ thể phục vụ cho đánh giá định tính hoặc định lượng.
Mẫu âm tính: không xuất hiện đường cong khuếch đại và không có giá trị Ct ở kênh tác nhân (No Ct = 0.00). Tuy nhiên, ở những mẫu này bắt buộc phải có tín hiệu khuếch đại ở kênh chứng nội, nhằm khẳng định phản ứng diễn ra bình thường.
Mẫu dương tính: có đường cong khuếch đại đặc trưng và giá trị Ct ở kênh tác nhân. Thông thường, cả kênh tác nhân và kênh chứng nội đều có tín hiệu. Trong một số tình huống, nếu giá trị Ct ở kênh tác nhân xuất hiện sớm, tín hiệu ở kênh chứng nội có thể không hiện rõ.
Mẫu nghi ngờ: theo TCVN, các mẫu có đường cong khuếch đại ở kênh tác nhân nhưng với giá trị Ct > 35 được xếp vào nhóm nghi ngờ. Những mẫu này cần được kiểm tra lại bằng Real-time PCR lần thứ hai hoặc bằng một phương pháp khác tương đương để xác nhận kết quả.
Không thể kết luận: khi cả kênh tác nhân và kênh chứng nội đều không có tín hiệu khuếch đại. Trường hợp này thường gợi ý sự hiện diện của chất ức chế phản ứng PCR; do đó cần pha loãng mẫu (ví dụ 1 mẫu: 9 PBS 1X) và tiến hành xét nghiệm lại.
EHP là tác nhân gây bệnh nguy hiểm trong nuôi tôm vì làm giảm tốc độ tăng trưởng và gây tổn thất kinh tế đáng kể, dù không gây chết hàng loạt. Việc chẩn đoán bằng các phương pháp truyền thống còn nhiều hạn chế do bào tử có kích thước rất nhỏ và triệu chứng trên tôm không đặc hiệu. Trong bối cảnh đó, Real-time PCR được xem là công cụ chẩn đoán chuẩn mực nhờ khả năng phát hiện nhanh, nhạy và đặc hiệu. Khi thực hiện đúng quy trình từ khâu thu và bảo quản mẫu, tách chiết vật liệu di truyền, thiết lập đối chứng đến phân tích và diễn giải kết quả, phương pháp này giúp giảm thiểu sai sót, nâng cao độ tin cậy và tạo cơ sở khoa học cho công tác giám sát, phòng ngừa cũng như quản lý dịch bệnh EHP trong thực tiễn nuôi tôm.
Tài liệu tham khảo
- Đỗ, N. Đ. T., Nguyễn, T. T. T., Nguyễn, D. K., & Phan, T. N. Đ. (2021). Kỹ thuật PCR và Real-time PCR: Từ lý thuyết đến thực hành. Nhà xuất bản Đại học Quốc gia Thành phố Hồ Chí Minh.
- Tiêu chuẩn quốc gia TCVN 8710-12:2019 về Bệnh thủy sản – Quy trình chẩn đoán – Phần 12: Bệnh vi bào tử do Enterocytozoon hepatopenaei ở tôm.
- World Organisation for Animal Health (WOAH). (2022). Infection with Enterocytozoon hepatopenaei (EHP) – Disease card.

