Trong nuôi tôm công nghiệp, EHP (Enterocytozoon hepatopenaei) gây bệnh chậm lớn và VPAHPND (Vibrio parahaemolyticus) gây hội chứng hoại tử gan tụy cấp là hai tác nhân gây thiệt hại nghiêm trọng, thường tồn tại ở nồng độ thấp trong giai đoạn sớm và khó phát hiện bằng các phương pháp truyền thống.
PCR kỹ thuật số vi giọt (droplet digital PCR – ddPCR) đang được xem là công nghệ tiềm năng nhờ khả năng phát hiện mục tiêu với độ nhạy và độ đặc hiệu cao. Bài viết này đánh giá độ nhạy và độ đặc hiệu của ddPCR nhằm phát hiện EHP và VPAHPND ở tôm. Từ đó giúp xác định hiệu quả của một phương pháp xét nghiệm nhằm nâng cao hiệu quả chẩn đoán dịch bệnh thủy sản.
Bài viết tham khảo kết quả nghiên cứu của nhóm tác giả Zhang và cộng sự (2022) trên tạp chí Journal of Fish Diseases [1]
1. ddPCR là gì?
Droplet digital PCR (ddPCR) là kỹ thuật PCR thế hệ mới, trong đó phản ứng được phân tách thành hàng chục nghìn vi giọt, cho phép định lượng tuyệt đối DNA/RNA mục tiêu mà không cần đường chuẩn. Điều này giúp ddPCR đặc biệt phù hợp cho các mẫu thủy sản có nền phức tạp và nồng độ mầm bệnh thấp.
2. Phương pháp đánh giá độ đặc hiệu của ddPCR
Độ đặc hiệu phản ánh khả năng phát hiện chính xác tác nhân mục tiêu mà không phát hiện các trình tự tương tự khác có trong mẫu.
Để đánh giá độ đặc hiệu của phương pháp PCR kỹ thuật số vi giọt trong việc phát hiện EHP và VPAHPND, mẫu tôm nhiễm các tác nhân gây bệnh khác nhau được thu thập bao gồm:
PC. Chứng dương
1. WSSV (White Spot Syndrome Virus) – virus gây bệnh đốm trắng
2. TSV (Taura Syndrome Virus) – virus gây hội chứng Taura
3. YHV(Yellow Head Virus) – virus gây bệnh đầu vàng
4. VH (Vibrio harveyi) – vi khuẩn gây bệnh phát sáng và nhiễm trùng đường ruột
5. DIV1 (Decapod Iridescent Virus 1) – virus DNA nguy hiểm gây ra bệnh DIV1
6. VP (Vibrio parahaemolyticus) – vi khuẩn gây bệnh hoại tử gan tụy cấp tính (AHPND)
7. NHPB (Necrotizing Hepatopancreatitis Bacterium) – vi khuẩn gây bệnh đốm đen
8. IHHNV (Infectious Hypodermal and Hematopoietic Necrosis Virus) – virus gây ra bệnh hoại tử dưới vỏ và cơ quan tạo máu ở tôm.
9. EHP (Enterocytozoon hepatopenaei) – vi bào tử trùng gây ra bệnh còi cọc trên tôm
10. VPAHPND (Vibrio parahaemolyticus) – vi khuẩn gây bệnh hoại tử gan tụy cấp tính
NC. Nước cất hai lần – đối chứng âm
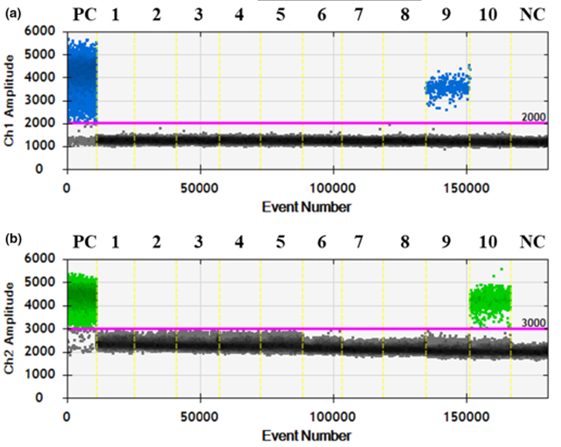
(a) tín hiệu của EHP kênh Ch1 (b) tín hiệu của VPAHPND kênh Ch2. Đường màu hồng ngưỡng phân biệt dương tính và âm tính.
Kết quả cho thấy: chứng dương (PC) ở cả 2 thử nghiệm đều cho kết quả dương tính và chứng âm (NC) đều âm tính không ghi nhận tín hiệu.
Mẫu tôm nhiễm EHP (hình 1a – Lane 9) và VPAHPND (hình 1b – Lane 10) cho kết quả dương tính rõ ràng với tín hiệu vượt ngưỡng trong đồ thị.
Các mẫu còn lại đều không ghi nhận tín hiệu cho thấy không có phản ứng chéo với các tác nhân khác như WSSV, TSV, YHV, DIV1 hay IHHNV. Kết quả này chứng minh rằng phương pháp ddPCR có độ đặc hiệu cao trong phát hiện EHP và VPAHPND trên tôm.
3. Phương pháp đánh giá độ nhạy của ddPCR
Độ nhạy phân tích là khả năng phát hiện được nồng độ rất thấp một mục tiêu có trong mẫu. Chỉ số này thường được biểu thị bằng giới hạn phát hiện (LOD – Limit of Detection) tức là nồng độ thấp nhất của mục tiêu mà xét nghiệm có thể phát hiện được một cách ổn định, thường đạt tỷ lệ ≥95% số mẫu.
Để đánh giá độ nhạy của kỹ thuật ddPCR trong phát hiện đồng thời EHP và VPAHPND, gene SWP1 của EHP và gene pirA của VPAHPND được tổng hợp và nối vào vector pUC57 tạo thành hai plasmid pUC57-EHP và pUC57-VPAHPND.
Các plasmid này được pha loãng bậc 10 bằng dung dịch TE 1X để tạo dải nồng độ chuẩn gồm:
| pUC57-EHP (chấm xanh dương) | pUC57-VPAHPND (chấm xanh lá) |
| 2.6×104 copies/ μL (Lane 1 & 2) 2.6×103 copies/ μL (Lane 3 & 4) 2.6×102copies/ μL (Lane 5 & 6) 2.6×101 copies/ μL (Lane 7 & 8) 2.6×100 copies/ μL (Lane 9 & 10) Chứng âm (Lane 11 & 12) | 5×104 copies/μL (Lane 1 & 2) 5×103 copies/μL (Lane 3 & 4) 5×102 copies/μL (Lane 5 & 6) 5×101 copies/μL (Lane 7 & 8) 5×100 copies/μL (Lane 9 & 10) Chứng âm (Lane 11 & 12) |
Mỗi nồng độ được phân cách bằng các đường màu vàng và lặp lại hai lần để xác định giới hạn phát hiện (LOD). Sau đó, nồng độ thấp nhất có thể phát hiện được được lặp lại 8 lần nhằm xác nhận độ nhạy phân tích của ddPCR.
Ngoài ra, các độ pha loãng tương tự cũng được thực hiện với mẫu DNA tôm không nhiễm EHP và VPAHPND để đánh giá xem DNA trong mẫu tôm có ảnh hưởng đến độ nhạy của ddPCR hay không.
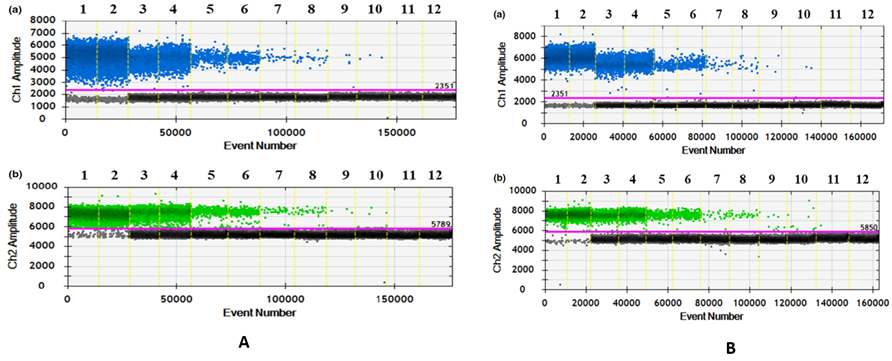
Phương pháp ddPCR cho thấy ngưỡng phát hiện thấp nhất của EHP khi pha loãng với TE là 2.6 copies/μL (Lane 10) và khi pha loãng với DNA tôm là 2.3 copies/μL (Lane 10). Tương tự, VPAHPND có thể được phát hiện ở nồng độ thấp nhất là 3.7 copies/μL khi pha với TE 1X và pha loãng với DNA tôm là 4.6 copies/μL. Điều này chứng minh ddPCR có độ nhạy cao phát hiện EHP và VPAHPND ở nồng độ thấp, nền mẫu khác nhau không ảnh hưởng đến độ nhạy của thử nghiệm.
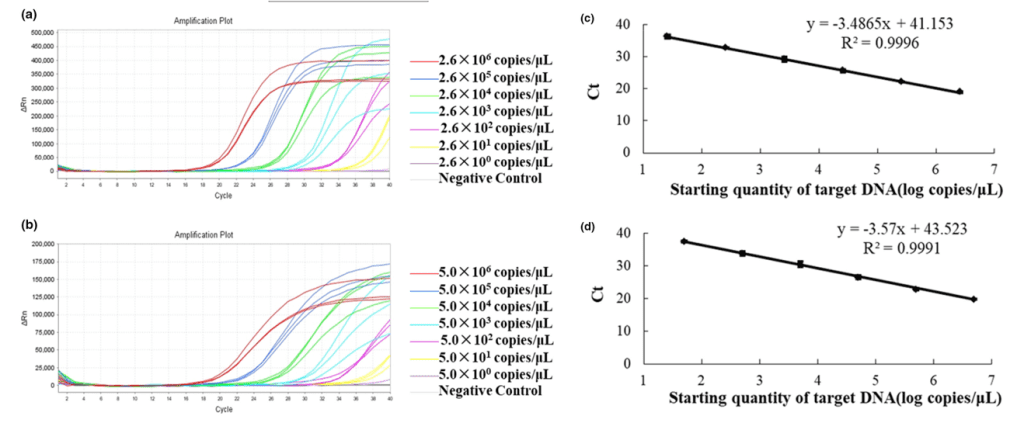
(a) Độ nhạy với EHP; (b) Độ nhạy với VPAHPND; (c) Đường chuẩn của EHP; (d) Đường chuẩn với VPAHPND
So sánh với phương pháp Real-time PCR định lượng, EHP chỉ được phát hiện ở ngưỡng thấp nhất là 2.6 × 10¹ copies/μL (Hình 3a đường màu vàng) và VPAHPND từ 5.0 × 10¹ copies/μL trở lên (Hình 3b đường màu vàng).
Mặc dù các phản ứng qPCR đều có hệ số tuyến tính (R²) > 0.999 chứng tỏ độ chính xác và tuyến tính cao, tuy nhiên độ nhạy phát hiện của qPCR vẫn thấp hơn khoảng 10 lần so với ddPCR đặc biệt ở các nồng độ cực thấp.
Không chỉ có độ nhạy và độ đặc hiệu cao, ddPCR không cần đường chuẩn, ít bị ảnh hưởng bởi chất ức chế trong mẫu và đặc biệt phù hợp cho phát hiện đồng thời nhiều tác nhân gây bệnh. Với những ưu điểm vượt trội, ddPCR đang trở thành xu hướng công nghệ xét nghiệm hiện đại trong ngành thủy sản, góp phần nâng cao hiệu quả và an toàn sinh học trong nuôi tôm công nghiệp.
Kết quả nghiên cứu cho thấy ddPCR là công cụ chẩn đoán hiệu quả trong phát hiện EHP và VPAHPND, vượt trội hơn qPCR về độ nhạy, đồng thời đảm bảo độ đặc hiệu cao. Đây là nền tảng quan trọng cho việc ứng dụng ddPCR trong quản lý dịch bệnh thủy sản hiện đại.
4. Tài liệu tham khảo
Zhang, H., Gong, H. Y., Cao, W. W., Que, M. Y., Ye, L., & Shi, L. (2022). Duplex droplet digital PCR method for the detection of Enterocytozoon hepatopenaei and Vibrio parahaemolyticus acute hepatopancreatic necrosis disease. Journal of fish diseases, 45(6), 761–769. https://doi.org/10.1111/jfd.13600.

