Nuôi tôm nước lợ trong những năm qua đã trở thành một ngành sản xuất hàng hóa hiệu quả cao, đóng vai trò chủ yếu trong việc thúc đẩy sản xuất kinh doanh của ngành nuôi trồng thủy sản. Đây cũng là một phần quan trọng trong chiến lược phát triển kinh tế của Việt Nam, mang lại nguồn thu ngoại tệ đáng kể.
Để đạt được sản lượng nuôi tôm hiệu quả cao, việc chẩn đoán và phòng trị bệnh trên tôm luôn được người dân và doanh nghiệp chú trọng từ khâu lựa chọn tôm giống postlarvae cho đến khi nuôi thương phẩm. Theo nghiên cứu của Bonami (2008) có hơn 20 loại bệnh do virus gây ra trên tôm, trong đó bệnh đốm trắng (WSSV), hội chứng Taura (TSV) và bệnh đầu vàng (YHV), bệnh hoại tử cơ quan tạo máu và lập biểu mô (IHHNV) là những bệnh thường gây thiệt hại lớn cho ngành nuôi tôm.
Trước đây, các bệnh do virus bị giới hạn bởi vùng địa lí giữa Tây và Đông bán cầu. Tuy nhiên, sự vận chuyển quốc tế tôm sống (phục vụ ngành nuôi tôm) và tôm chết (nguyên liệu chế biến thuỷ sản và thương mại) đã dẫn đến sự lan truyền một số bệnh từ Tây bán cầu. Cụ thể, tôm nguyên liệu đông lạnh được cho là con đường lan truyền WSSV từ Châu Á sang Trung Mỹ, trong khi TSV lây lan theo hướng ngược lại (thông qua tôm giống từ các nước Trung Mỹ).
Với chi phí tổn thất hàng năm do dịch bệnh (chủ yếu là bệnh do virus) lên đến hàng tỉ USD mỗi năm, việc chẩn đoán sớm và kiểm soát dịch bệnh luôn được quan tâm và đề cao. Bài viết này sẽ cung cấp cho độc giả những thông tin về bệnh đốm trắng trên tôm, cơ chế gây nhiễm bệnh và các phương pháp trong chẩn đoán, phòng chống.
1. Đặc điểm bệnh đốm trắng trên tôm (WSSV)
Bệnh đốm trắng do virus White Spot Syndrome Virus (WSSV) thuộc chi Whispovirus, họ Nimaviridae gây ra. Virus gây hội chứng đốm trắng (WSSV) được phát hiện đầu tiên vào năm 1992 tại Đài Loan sau đó là Nhật Bản và Hàn Quốc. Sau đó, bệnh lây lan sang Malaysia, Ấn Độ và Thái Lan vào năm 1994, và gây thiệt hại khắp Đông Nam Á năm 1996.

Virus gây bệnh đốm trắng có dạng hình que, kích thước vỏ dài 240 – 380 nm đường kính 70 – 159 nm, phần lõi nucleocapsid dài 120 – 205 nm với đường kính 95 – 165 nm. Virus này có DNA sợi kép, chiều dài DNA gần bằng 290 kb. Kích cỡ bộ gene thay đổi theo từng vùng địa lí như dạng WSSV ở Thái Lan là 293 kb, Trung Quốc là 305 kb và dòng WSSV ở Đài Loan là 307 kb.
Độc lực của WSSV phụ thuộc vào loài cảm nhiễm và khác nhau ở các dòng virus. Ví dụ như đối với tôm thẻ chân trắng, dòng virus Texas có tính độc cao nhất so với các dòng khác tỷ lệ tôm chết đến 100% khi nhiễm virus. Ngoài ra, khả năng gây độc và tính cạnh tranh của virus còn phụ thuộc vào kích thước của bộ gene. Dòng virus WSSV (WSSV-TH-96-II, kích thước bộ gene 312 kb) có thời gian gây chết trên tôm (LT50) là 14 ngày, chậm hơn so với dòng virus WSSV-TH (kích thước bộ gene là 292 kb) có LT50 là 3,5 ngày. Sự khác biệt này được giải thích dựa trên tốc độ sao chép của virus trong tế bào chủ sau khi bị xâm nhiễm.
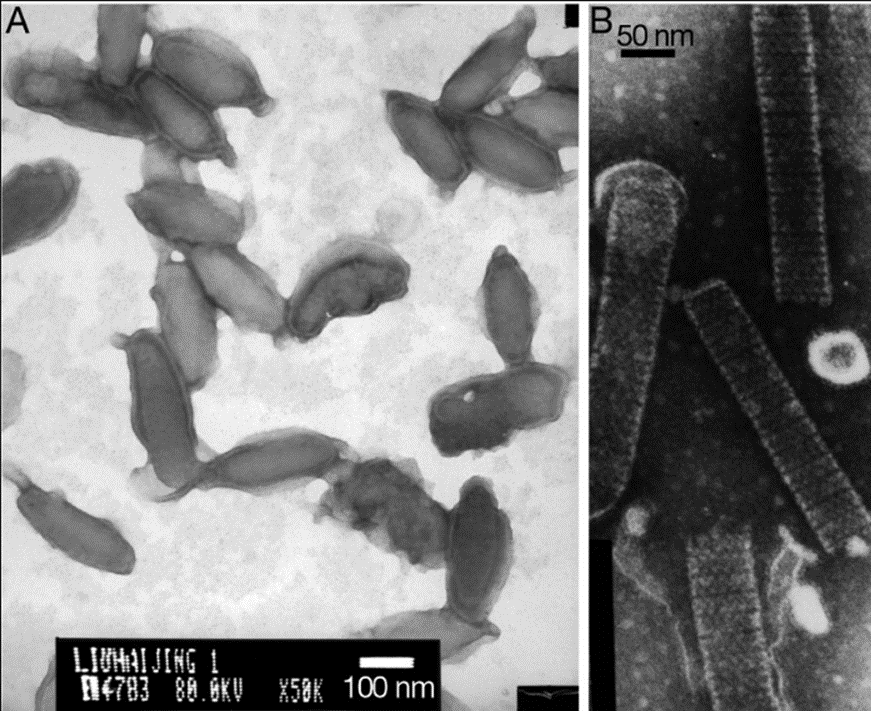
Các protein của WSSV rất phức tạp. Hạt virion có ít nhất 45 loại protein cấu trúc. Nucleocapsid có cấu trúc dạng que, xoắn (70 × 300 nm) chứa DNA mạch đôi dạng vòng và 9 loại protein bên trong lõi. Nucleocapsid gồm một protein VP15 và một protein lớn VP664, hình thành nên các tiểu đơn vị dạng vòng chồng lên nhau. Lớp vỏ (tegument) liên kết với nucleocapsid và màng bao. Lớp vỏ chứa ít nhất 4 protein cấu trúc (VP26, VP36A, VP39A, VP95). Màng bao ngoài cùng dày 6 – 7 nm bao gồm 3 lớp lipid và chứa ít nhất 28 loại protein, nhiều loại protein có các domain xuyên màng. Trong số đó, protein VP28 giữ vai trò quan trọng trong quá trình xâm nhiễm hệ thống (systemic infection) và đã được chứng minh gây đáp ứng bảo vệ trên tôm bị nhiễm.
2. Khả năng chống chịu các điều kiện từ môi trường
Trong các nghiên cứu trong phòng thí nghiệm, WSSV bị bất hoạt trong các điều kiện sau:
- Nhiệt: 55°C trong 90 phút, 70°C trong 5 phút (Chang và cộng sự, 1998); 50°C trong 60 phút; 60°C trong 1 phút; 70°C trong 0,2 phút (Nakano và cộng sự, 1998).
- Làm khô: WSSV hấp phụ trên giấy lọc và để khô sau đó bị bất hoạt trong 1 giờ ở 30°C và trong 3 giờ ở 26°C (Maeda và cộng sự, 1998; Nakano và cộng sự, 1998).
- pH: pH 3 trong 60 phút; pH 12 trong 10 phút (Balasubramanian và cộng sự, 2006; Chang và cộng sự, 1998).
- Tia cực tím: Tổng liều 9,30 × 105 µWs/cm2 (Chang và cộng sự, 1998).
- Ozone: Tổng nồng độ chất oxy hóa còn lại là 0,5 µg ml–1 trong 10 phút (Chang và cộng sự, 1998).
- Natri hypochlorite: Tổng nồng độ clo tự do là 100 ppm trong 10 phút (Chang và cộng sự, 1998).
- Benzalkonium clorua: 100 ppm trong 10 phút (Balasubramanian và cộng sự, 2006).
- Iodophore: Tổng nồng độ iốt tự do là 100 ppm trong 10 phút (Chang và cộng sự, 1998).
3. Các cơ quan đích và mô bị nhiễm bệnh
Các mô mục tiêu chính của WSSV có nguồn gốc phôi ngoài da (mang, chân bơi, cơ thịt) và trung bì, đặc biệt là biểu mô biểu bì và mô liên kết dưới da (Momoyama và cộng sự, 1994; Wu và cộng sự, 2013). Mặc dù WSSV lây nhiễm vào mô liên kết bên dưới ở gan tụy và ruột giữa giáp xác, tuy nhiên, tế bào biểu mô ống của hai cơ quan này có nguồn gốc nội bì nên không bị nhiễm trùng.
4. Kiểm soát và phòng ngừa WSSV
Mặc dù về cơ chế cơ bản vẫn chưa được làm rõ nhưng một số thí nghiệm tại phòng thí nghiệm đã chỉ ra rằng tôm thẻ và tôm càng được tiêm phòng có tỷ lệ sống sót cao hơn sau khi bị nhiễm WSSV. Lần đầu tiên người ta chứng minh rằng tôm Penaeus japonicus sống sót sau khi nhiễm WSSV tự nhiên và thử nghiệm đã thể hiện khả năng kháng lại WSSV ở lần gây nhiễm sau đó (Venegas và cộng sự, 2000). Các nghiên cứu sau này cho thấy rằng sau khi thực hiện tiêm phòng vào các mô cơ các virion WSSV bất hoạt hoặc các dạng protein tái tổ hợp (VP28), đã tăng cường khả năng chống nhiễm WSSV trong các thí nghiệm.
Hơn nữa, tôm được nuôi bằng thức ăn viên dạng nấm men tái tổ hợp với protein VP28 cho thấy tỷ lệ sống sót tốt hơn khi cho thử nhiễm với WSSV (Witteveldt et al., 2004). Tuy nhiên, những kết quả hứa hẹn này chỉ có hiệu quả khi tôm bị nhiễm WSSV với tải lượng thấp. Ngoài ra, tác dụng thường chỉ kéo dài trong vài ngày hoặc trong trường hợp tôm càng là khoảng 20 ngày.
Một biện pháp tiềm năng khác để bảo vệ tôm khỏi bị nhiễm WSSV là sử dụng phương pháp can thiệp RNA (RNAi). Các RNA chuỗi kép (ds) đặc hiệu gene WSSV tạo ra hoạt tính kháng WSSV mạnh mẽ, bảo vệ tôm chống lại nhiễm WSSV, nhưng nghiên cứu tương tự cho thấy rằng dsRNA dài gây ra cả phản ứng kháng virus độc lập và phụ thuộc vào trình tự ở tôm (Robalino và cộng sự, 2005). Một nghiên cứu gần đây hơn cho thấy rằng ngay cả khi dùng đường uống VP28 dsRNA được biểu hiện bằng vi khuẩn cũng có thể bảo vệ tôm chống lại nhiễm WSSV (Sarathi và cộng sự, 2008). Tuy nhiên, mặc dù công nghệ dsRNA vẫn tiếp tục được nghiên cứu nhưng vẫn chưa có dữ liệu thử nghiệm thực địa về phương pháp tiêm chủng hoặc phương pháp RNAi.
5. Tiềm năng của các giải pháp phòng chống kiểm soát dịch khi ứng dụng trên tôm
1. Tiêm phòng thử nghiệm
Không có phương pháp tiêm chủng hiệu quả nhất quán nào được phát triển để điều trị nhiễm WSSV.
2. Sử dụng hóa chất để điều trị
Không có phương pháp được công bố hoặc xác nhận.
3. Kích thích miễn dịch
Một số báo cáo đã chỉ ra rằng beta-glucan, vitamin C, chiết xuất rong biển (Fucoidan) và các chất kích thích miễn dịch khác có thể cải thiện khả năng chống nhiễm WSSV (Chang và cộng sự, 2003; Chotigeat và cộng sự, 2004).
4. Nhân giống kháng bệnh
Tiến bộ trong việc nhân giống P. vannamei để chống lại nhiễm WSSV đã được báo cáo (Cuéllar-Anjel et al., 2012; Huang et al., 2012).
5. Tái đàn với các loài kháng bệnh
Không áp dụng cho trường hợp nhiễm WSSV
6. Thuốc
Không có thuốc hiệu quả nào có thể được đề xuất tại thời điểm này. rVP28 có tác dụng nhưng nó chưa thể được sử dụng như một tác nhân ngăn chặn thực tế.
7. Khử trùng trứng và ấu trùng
Đối với sự lây truyền qua trứng, việc khử trùng trứng có thể có hiệu quả (Lo & Kou, 1998), nhưng điều này vẫn chưa được xác nhận trong các thử nghiệm khoa học chính thức.
8. Thực hành chăn nuôi, nuôi trồng chung
Một số biện pháp chăn nuôi đã được áp dụng thành công để quản lý nhiễm WSSV, chẳng hạn như tránh thả giống vào mùa lạnh, sử dụng nguồn giống không có mầm bệnh (SPF) hoặc phản ứng chuỗi polymerase (PCR), sử dụng nước và nuôi cấy an toàn sinh học (Withyachumnarnkul, 1999) và nuôi ghép tôm cá (He et al., dữ liệu chưa được công bố).
6. Đánh giá các phương pháp xét nghiệm theo Tổ chức Thú y thế giới (WOAH)
Các phương pháp hiện có để chẩn đoán nhiễm WSSV được liệt kê trong Bảng 1.
Bảng 1: Kết quả đánh giá các phương pháp chẩn đoán bệnh WSSV.
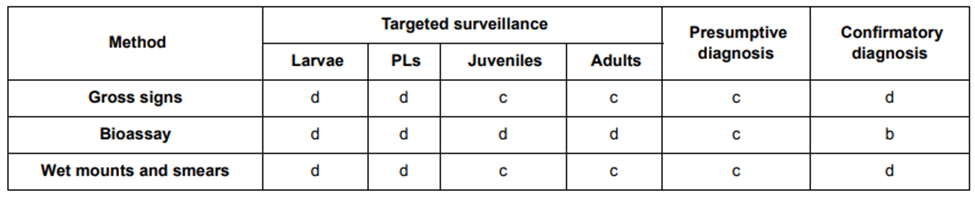

Ký hiệu chữ cái được sử dụng trong bảng chỉ ra:
a = Phương pháp được khuyến nghị vì lý do sẵn có, tiện ích, độ đặc hiệu và độ nhạy chẩn đoán
b = Phương pháp tiêu chuẩn có độ nhạy và độ đặc hiệu chẩn đoán tốt
c = Phương pháp được áp dụng trong một số trường hợp, nhưng chi phí, độ chính xác hoặc các yếu tố khác có hạn chế khi áp dụng
d = Phương pháp này hiện không được khuyến nghị cho mục đích này
Dựa vào đánh giá có thể thấy Real-time PCR là một trong những phương pháp tiềm năng khi được khuyến nghị sử dụng hầu hết ở các quá trình chẩn đoán trên các giai đoạn của tôm.
Quy trình xét nghiệm, chẩn đoán của ABT trên bệnh đốm trắng tôm WSSV

► Kit tách chiết DNA/RNA bằng phương pháp tách thô
TopPURE® CRUDE DNA EXTRACTION KIT (EXS-011) sử dụng cho tách chiết thô DNA từ virus trong mẫu mô (tôm, cá,..) và vi khuẩn nuôi cấy.
► Kit tách chiết DNA/RNA bằng phương pháp tách cột Silica
TopPURE® HIGHPURE VIRAL EXTRACTION KIT (EXS-021) sử dụng cho tách chiết DNA/RNA từ mẫu tôm bằng phương pháp cột silica.
TopPURE® FLUID VIRAL DNA/RNA EXTRACTION KIT CE (HI-712) sử dụng cho tách chiết DNA/RNA từ mẫu tế bào nuôi cấy, vi khuẩn, huyễn dịch (huyền phù), mẫu quét bề mặt, mẫu dịch phết (y tế).
► Kit tách chiết DNA/RNA bằng phương pháp tách hạt từ
TopPURE® Maga Genomic DNA/RNA EXTRACTION KIT CE (HI-612) sử dụng cho tách chiết DNA/RNA từ tế bào nuôi cấy, vi khuẩn gram (-) và gram (+), huyễn dịch (huyền phù), mẫu quét bề mặt, mẫu dịch phết bao gồm SARS-CoV-2 bằng phương pháp tách chiết từ tự động.
► Phương pháp tách từ thủ công
TopPURE® MANUAL MAGA GENOMIC DNA/RNA KIT sử dụng cho tách chiết DNA/RNA từ tế bào nuôi cấy, vi khuẩn gram (-) và gram (+), huyễn dịch (huyền phù), mẫu quét bề mặt, mẫu dịch phết bao gồm SARS-CoV-2 bằng phương pháp tách chiết từ tự động.
► PCR và Real-time PCR
Kit Real-time PCR: TopSPEC® WSSV qPCR KIT (SQS-112) phát hiện tác nhân gây bệnh đốm trắng WSSV trên mẫu tôm bằng kỹ thuật Real-time PCR.

