Xét nghiệm trước sinh không xâm lấn (NIPT) là kỹ thuật sàng lọc DNA của thai nhi lưu hành tự do (cffDNA) trong huyết tương của mẹ nhằm mục đích xác định các bất thường về nhiễm sắc thể của thai nhi. Bài viết này sẽ trình bày Panel ứng dụng công nghệ PCR kỹ thuật số (dPCR) trong xét nghiệm NIPT để xác định các đột biến của thai nhi. Từ đó cho phép sàng lọc trước sinh ở thời điểm sớm hơn, giảm nguy cơ sảy thai do phải sử dụng các biện pháp xâm lấn như chọc ối hay sinh thiết.
1. Tổng quan kỹ thuật sàng lọc trước sinh không xâm lấn NIPT
1.1. Bất thường nhiễm sắc thể và hội chứng di truyền phổ biến
Ở người, các bất thường liên quan đến số lượng và cấu trúc nhiễm sắc thể gây ra các hội chứng di truyền nghiêm trọng. Ví dụ, các bệnh liên quan đến thể lệch bội phổ biến như thể ba (trisomy), chủ yếu bao gồm thể ba 21, 18 và 13 gây ra hội chứng Down, hội chứng Edwards và hội chứng Patau.
1.2. NIPT là gì? Ứng dụng PCR kỹ thuật số (dPCR) trong xét nghiệm NIPT là gì?
Tiêu chuẩn vàng để chẩn đoán các rối loạn này là xét nghiệm nhiễm sắc thể của thai nhi thông qua Sinh thiết gai nhau (CVS – Chorionic Villus Sampling) hoặc chọc ối (Amniocentesis). Tuy nhiên, các phương pháp xâm lấn này có tỷ lệ rủi ro thấp như sảy thai và nhiễm trùng tử cung.
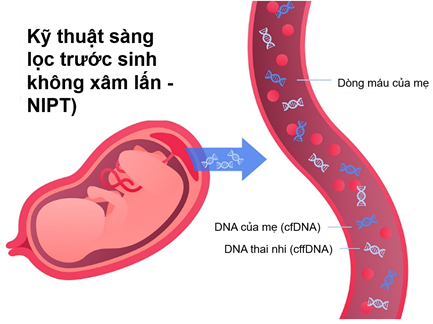
NIPT là kỹ thuật xét nghiệm trước sinh không xâm lấn, an toàn để phát hiện các đoạn DNA thai nhi lưu hành tự do (cffDNA) trong máu mẹ. NIPT dựa trên kỹ thuật giải trình tự thế hệ mới NGS có độ nhạy và độ đặc hiệu cao để tầm soát và phát hiện các biến thể di truyền. Tuy nhiên, phương pháp này gặp thách thức về chi phí, trang thiết bị phức tạp và hạn chế phân tích các mẫu có lượng cffDNA thai nhi thấp – đặc biệt trong giai đoạn đầu thai kỳ hoặc các trường hợp liên quan đến đột biến di truyền từ mẹ.
Gần đây, PCR kỹ thuật số (dPCR) là phương pháp giá trị trong phát hiện tình trạng bất thường của thai nhi nhờ vào khả năng định lượng tuyệt đối axit nucleic. Phương pháp này không xâm lấn, có độ chính xác và độ nhạy cao nhằm phát hiện được tỷ lệ cffDNA thấp trong huyết tương của mẹ. Quy trình thực hiện dPCR đơn giản, phân tích dữ liệu nhanh và thời gian xử lý ngắn hơn so với phương pháp NGS khiến nó trở thành một công cụ đầy hứa hẹn cho các khoa lâm sàng.
2. Ứng dụng dPCR trong xét nghiệm NIPT phát hiện β-thalassemia bệnh tan máu bẩm sinh Thalassemia
2.1. Tổng quan bệnh tan máu bẩm sinh β-thalassemia
β-thalassemia là một rối loạn máu di truyền lặn trên nhiễm sắc thể thường liên quan đến tình trạng thiếu (β0 ) hoặc giảm (β+ ) hemoglobin gây ra tình trạng thiếu máu nặng. Việc sàng lọc, chẩn đoán, điều trị trước sinh và sơ sinh để phát hiện, can thiệp và điều trị sớm trong giai đoạn bào thai và sơ sinh giúp cho trẻ sinh ra phát triển bình thường hoặc tránh được những hậu quả nặng nề về thể chất và trí tuệ, giảm thiểu số người tàn tật, thiểu năng trí tuệ trong cộng đồng, góp phần nâng cao chất lượng dân số.
2.2. Quy trình thực hiện dPCR trong NIPT thalassemia
Theo khuyến cáo của Bộ y tế (2020), xét nghiệm DNA thai nhi lưu hành trong máu mẹ (kỹ thuật sàng lọc trước sinh không xâm lấn – NIPT) để sàng lọc các bất thường nhiễm sắc thể của thai nhi được thực hiện ≥ 10 tuần sau khi có kết quả siêu âm thai và được chuyên gia tư vấn di truyền tư vấn để có chỉ định phù hợp.
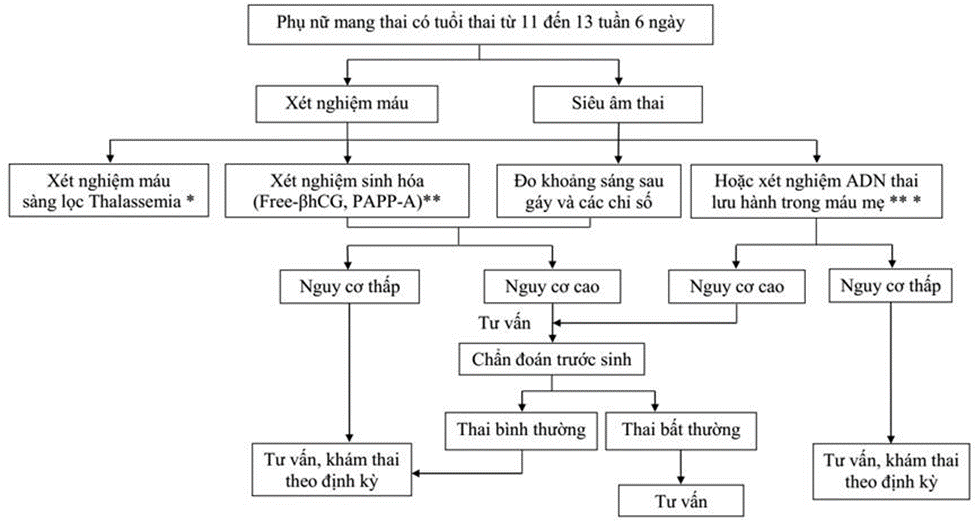
*: Thực hiện theo quy trình tại sơ đồ 1. Sàng lọc, chẩn đoán bệnh tan máu bẩm sinh Thalassemia.
**: Chỉ thực hiện ở các cơ sở đủ điều kiện.
***: Có thể sử dụng để sàng lọc bổ sung khi có kết quả xét nghiệm sinh hóa/huyết thanh nguy cơ cao.
Hai đột biến phổ biến nhất của β-thalassemia là β+ IVSI-110 (đột biến vị trí ghép nối) và β0 39 (đột biến codon vô nghĩa). Xét nghiệm NIPT dựa trên dPCR cho các đột biến nêu trên (di truyền từ mẹ hoặc từ cha) bằng cách phân tích kiểu gen thai nhi được thực hiện theo quy trình sau:
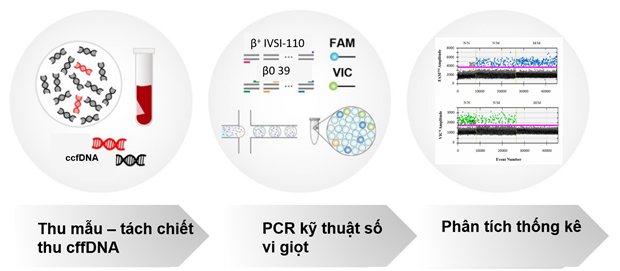
(1) Thu thập mẫu:
Các mẫu máu từ phụ nữ mang thai ở các độ tuổi thai khác nhau (tuần thứ 5–39 của thai kỳ) được thu thập bằng ống nghiệm chứa chất chống đông EDTA.
Trong huyết tương của phụ nữ mang thai, tỷ lệ cffDNA thường nằm trong khoảng từ 3% đến 10–20% tổng số cfDNA. Tiến hành mô phỏng sự phân mảnh cfDNA bằng cách xử lý với enzyme cắt giới hạn SspI trước khi tiến hành thí nghiệm dPCR. cfDNA được tách chiết từ 2 mL huyết tương của mẹ bằng bộ kit thương mại chuyên dụng.
(2) Thực hiện PCR kỹ thuật số:
Tuỳ thuộc vào công nghệ khác nhau lựa chọn hệ thống PCR kỹ thuật số phù hợp. Các công nghệ PCR kỹ thuật số phổ biến là kỹ thuật tạo vi giọt nhũ tương – dầu (ddPCR), công nghệ vi chip (cdPCR) và PCR kỹ thuật số vi lưu (mdPCR).
Quy trình sau thực hiện dựa trên kỹ thuật số vi giọt ddPCR trên hệ thống PCR QX200™ Droplet Digital™ (Bio-Rad). Bộ mồi/đầu dò thiết kế để phát hiện đột biến β+ IVSI-110, β0 39 hoặc cả hai đột biến. Kênh màu FAM™ phát hiện alen đột biến (M) và kênh màu VIC® phát hiện alen bình thường (N)
Kết quả được phân tích bằng phần mềm QuantaSoft 1.3.2.0 (Bio-Rad) để thu thập dữ liệu và tính toán nồng độ tuyệt đối của DNA mục tiêu (theo copies/μL phản ứng) bằng phân phối Poisson
Đọc thêm: Hướng dẫn thực hiện PCR kỹ thuật số (dPCR) dựa trên chip và trên giọt hay nhũ tương
(3) Phân tích thống kê:
Sau khi xác định số lượng giọt dương tính, giọt âm tính và giọt dương tính kép, để xác định tình trạng bệnh của mẫu thử nghiệm, tỷ lệ giữa tổng số bản sao của alen đột biến với tổng số bản sao của alen kiểu hoang dã (RM:N ) và z-score được tính toán.
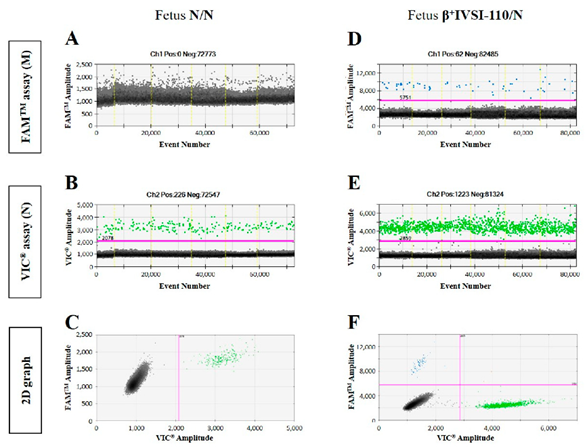
Chấm đen: giọt không chứa DNA đích; chấm xanh lá: alen bình thường; chấm xanh dương: alen đột biến; đường màu hồng: ngưỡng cường độ huỳnh quang để phân biệt giọt dương và âm tính.
Dựa vào kết quả trên, kỹ thuật NIPT dựa trên công nghệ ddPCR cung cấp một quy trình sàng lọc đơn giản, nhanh chóng và nhạy để xác định đột biến thalassemia β+ IVSI-110 và β0 39 di truyền từ cha và lần đầu tiên được thừa hưởng từ mẹ. dPCR hiện nay cũng được ứng dụng để sàng lọc chẩn đoán các bệnh di truyền khác như lệch bội nhiễm sắc thể, mất đoạn, nhân đôi NST, thiếu máu hồng cầu hình liềm, máu khó đông, teo cơ tuỷ sống,… để sàng lọc xem thai nhi có thể có số lượng nhiễm sắc thể bất thường hay không.
Mặc dù dPCR có lợi thế về chi phí và tốc độ, nhưng cần phải phát triển thêm để mở rộng ứng dụng của nó vào sàng lọc lệch bội nhiễm sắc thể toàn diện. Cần chuẩn hóa các phương pháp phát hiện, mở rộng khả năng chạy multiplex, cải thiện việc xử lý mẫu và tích hợp tin sinh học để thiết kế đầu dò tốt hơn, thúc đẩy chăm sóc sức khỏe bà mẹ và thai nhi và giải quyết những hạn chế của các phương pháp chẩn đoán hiện tại.
3. Tài liệu tham khảo
- Bộ Y tế. (2020). Quyết định số 1807/QĐ-BYT: Về việc ban hành hướng dẫn về chuyên môn kỹ thuật trong sàng lọc, chẩn đoán, điều trị trước sinh và sơ sinh. Quyết định 1807/QĐ-BYT 2020 chuyên môn kỹ thuật sàng lọc chẩn đoán điều trị trước sinh sơ sinh
- D’Aversa, E., Breveglieri, G., Boutou, E., Balassopoulou, A., Voskaridou, E., Pellegatti, P., Guerra, G., Scapoli, C., Gambari, R., & Borgatti, M. (2022). Droplet Digital PCR for Non-Invasive Prenatal Detection of Fetal Single-Gene Point Mutations in Maternal Plasma. International Journal of Molecular Sciences, 23(5), 2819. https://doi.org/10.3390/ijms23052819
- Guo, Y., Charoenkwan, P., Traisrisilp, K., Piyamongkol, W., & Tongprasert, F. (2025). Application of Digital Polymerase Chain Reaction (dPCR) in Non-Invasive Prenatal Testing (NIPT). Biomolecules, 15(3), 360. https://doi.org/10.3390/biom15030360
- Tan, C., Chen, X., Wang, F., Wang, D., Cao, Z., Zhu, X., … Zhu, L. (2019). A Multiplex Droplet Digital PCR Assay for Non-invasive Prenatal Testing of Fetal Aneuploidy. The Analyst. doi:10.1039/c8an02018c
