Real-time PCR định lượng (qPCR) là kỹ thuật được sử dụng phổ biến trong các lĩnh vực xét nghiệm chẩn đoán lâm sàng để định lượng chính xác axit nucleic mục tiêu có trong mẫu. Để thực hiện xét nghiệm Real-time PCR thành công, quá trình khuếch đại sản phẩm phải hiệu quả và có độ đặc hiệu cao. Cả mồi và đầu dò đều có thể ảnh hưởng đến hiệu quả và độ đặc hiệu của quá trình khuếch đại và do đó ảnh hưởng đến độ chính xác của xét nghiệm Real-time PCR. Vì vậy, cần phải lựa chọn kỹ lưỡng trình tự mục tiêu, thiết kế mồi và đầu dò một cách cẩn thận và chính xác để đảm bảo kết quả real-time PCR đạt độ chính xác.
Khi thiết kế mồi và đầu dò cho xét nghiệm Real-time PCR định lượng cần thực hiện theo các bước sau:
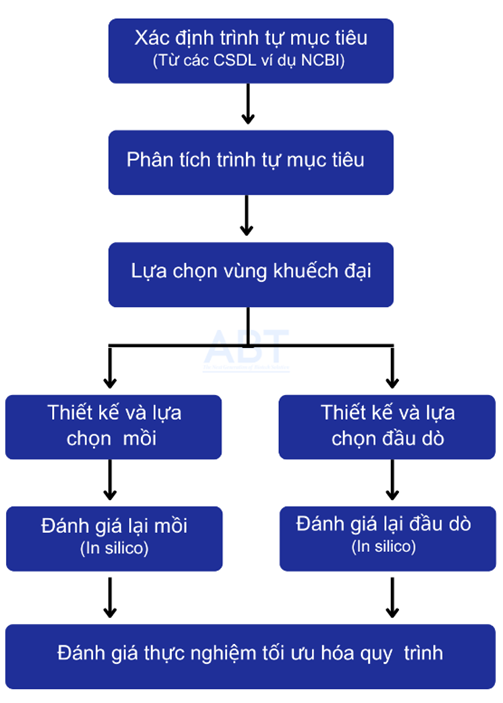
Xác định trình tự mục tiêu
Trước khi tiến hành thiết kế mồi/đầu dò cho phản ứng real-time PCR cần xác định trình tự mục tiêu cụ thể cần khuếch đại. Trình tự mục tiêu này cần có sự ổn định di truyền, độ bảo tồn cao và có tính chuyên biệt so với trình tự của vi sinh vật khác. Sau khi lựa chọn trình tự mục tiêu đã hoàn tất, bước tiếp theo là tìm các vùng nhắm mục tiêu bằng cách thủ công căn chỉnh trình tự hoặc xếp gióng cột tự động bằng các phần mềm chuyên dụng.
Một số hướng dẫn để lựa chọn trình tự cần khuếch đại phù hợp bao gồm:
- Sản phẩm khuếch đại có kích thước từ 75 – 200 bp.
- Tránh thiết kế vào các vùng có cấu trúc thứ cấp.
- Tránh các vùng có các đoạn lặp lại dài (>4) của các nucleotide.
- Chọn vùng có hàm lượng GC từ 50–60%, tránh các vùng giàu GC trong trình tự mục tiêu vì chúng khó khuếch đại.
Có một số tài công cụ trực tuyến miễn phí giúp xác định trình tự mục tiêu như NCBI (https://www.ncbi.nlm.nih.gov/gene?cmd=search), Viện Sanger/Viện tin sinh Châu Âu (https://asia.ensembl.org/index.html) hoặc tham khảo từ các nghiên cứu khoa học đã công bố để tìm kiếm các gene mục tiêu tiềm năng.
Nguyên tắc thiết kế mồi cho cho phản ứng Real-time PCR định lượng
- Độ dài của mồi: Kích thước tối ưu của các đoạn mồi thường nằm trong khoảng từ 15 đến 30 nucleotide. Thiết kế mồi quá ngắn, làm giảm độ đặc hiệu của phản ứng real-time PCR. Ngược lại, mồi dài có thể liên kết tốt với trình tự mục tiêu, nhưng quá dài làm giảm hiệu quả khuếch đại PCR dẫn đến giảm năng suất và chất lượng của sản phẩm real-time PCR định lượng.
- Nhiệt độ nóng chảy của mồi Tm: Là thông số rất quan trọng ở giai đoạn gắn mồi. Tm được định nghĩa là điểm nhiệt tại đó 50% sợi đôi ADN phân tách nhau tạo sợi đơn. Giá trị Tm của các đoạn mồi nên nằm trong khoảng từ 55 đến 60°C . Ngoài ra, Tm giữa mồi xuôi và mồi ngược không được lệch nhau hơn 2°C.
- Nhiệt độ gắn mồi (Ta): Là nhiệt độ mồi gắn lên DNA khuôn, được tính toán dựa vào nhiệt độ nóng chảy Tm của mồi. Ta thường thấp hơn Tm khoảng 3-5oC. Ta quá cao sẽ tạo ra quá trình bắt cặp bổ sung giữa mồi và mẫu không đủ dẫn đến nồng độ sản phẩm PCR thấp. Ta quá thấp có thể dẫn đến các sản phẩm không đặc hiệu.
- Hàm lượng GC: Thiết kế các đoạn mồi có hàm lượng GC từ 50–60%. Tránh các vùng nhiều nu C và G trong các đoạn mồi vì chúng có thể tạo nên cấu trúc tetraplex, rất ổn định và không thể được phiên mã bởi polymerase.
- Kẹp GC: Chọn các đoạn mồi chỉ có một hoặc hai nu G/C trong năm nucleotide cuối cùng ở đầu 3′. Hàm lượng GC quá cao ở đầu 3’ của mồi có thể gây liên kết đầu 3’ quá mạnh khiến mồi bắt cặp không đặc hiệu làm giảm tính đặc hiệu của phản ứng. Mồi nên có ít nhất một G hoặc C ở đầu 3′ đảm bảo liên kết chính xác và mạnh với khuôn mẫu.
- Tránh cấu trúc thứ cấp: Đây là một hiện tượng phổ biến trong phản ứng real-time PCR khi hai mồi tự liên kết với nhau thay vì với khuôn mẫu, đặc biệt là gần đầu 3′. Các cấu trúc thứ cấp như kẹp tóc, primer-dimer, tương đồng chéo, lặp có thể được hình thành và gây ra hiện tượng dương tính giả hoặc ảnh hưởng đến cường độ tín hiệu kết quả, vì vậy cần tránh tạo các cấu trúc này nhất có thể khi thiết kế.
Nguyên tắc thiết kế đầu dò cho phản ứng real-time PCR định lượng
Đầu dò TaqMan là một loại đầu dò đánh dấu huỳnh quang phổ biến sử dụng trong Real-time PCR để phát hiện và định lượng một hoặc nhiều tác nhân mục tiêu có trong mẫu. Khi thiết kế đầu dò TaqMan cần lưu ý các đặc điểm sau:
Độ dài của đầu dò: Chiều dài đầu dò nên từ 18-30 nucleotide và tối ưu nhất ở 23 nu. Việc sử dụng đầu dò quá dài ảnh hưởng đến độ nhạy, sự dập tắt tín hiệu huỳnh quang kém hiệu quả hơn tạo ra tín huỳnh quang thấp. Trong khi việc sử dụng các đầu dò quá ngắn làm giảm độ đặc hiệu của phản ứng.
Nhiệt độ nóng chảy của đầu dò Tm: Tm của đầu dò phải cao hơn 8–10°C so với các đoạn mồi vì đầu dò sẽ liên kết với mạch khuôn trước các mồi xuôi và mồi ngược trong quá trình khuếch đại.
Hàm lượng GC: Tỷ lệ GC từ 30 đến 80%. Nucleotide đầu tiên ở đầu 5′ của đầu dò không thiết kế nu G để tránh hiện tượng dập tắt tín hiệu ngay cả sau khi đầu dò phân cắt, dẫn đến giảm giá trị tín hiệu huỳnh quang. Hơn nữa, đầu dò phải chứa nhiều C hơn G cho phép các tín hiệu dương tính thấp có thể dễ dàng phân biệt hơn với tín hiệu nền
Cấu trúc thứ cấp: Đầu dò cần tránh cấu trúc thứ cấp, ngoài ra không được chồng lên hoặc bổ sung cho bất kỳ đoạn mồi nào.
Lựa chọn Reporter và quencher thích hợp: Lựa chọn reporter và quencher cần xem xét ba tiêu chí: (a) các đầu dò phải được gắn reporter có phổ huỳnh quang tách biệt tốt hoặc chỉ có sự chồng chéo tối thiểu, (b) kết hợp reporter và quencher phải tương thích với khả năng phát hiện của thiết bị real-time PCR và (c) nên sử dụng quencher dạng không huỳnh quang. Tham khảo các chất reporter và quencher tại bài viết Vì sao lựa chọn Taqman probe cho Real-time PCR?
Các thông số tiêu chuẩn khi thiết kế mồi/đầu dò cho phản ứng real-time PCR được tóm tắt trong bảng sau:
| Yếu tố | Primers | Probes |
| Chiều dài | Chiều dài 15-30 Nu và độ dài tối ưu là khoảng từ 18-22 nu | Chiều dài 18-30 Nu và tối ưu nhất ở 23 nu. |
| %GC | Dao động từ 50-60% | Dao động từ 30-80% |
| Đặc điểm trình tự | Không nên để liên tiếp 3 nu GGG liên tiếp nhau. Mồi xuôi và mồi ngược không cách quá xa nhau. 5 nu ở đầu kết thúc 3’ không nhiều hơn 2 G,C | Không nên để liên tiếp 3 nu GGG liên tiếp nhau. Không nên có G ở đầu kết thúc 5’ Chứa nhiều C hơn G |
| Nhiệt độ nóng chảy (Tm) | Nằm trong khoảng từ 50-60℃. Tm giữa mồi xuôi và mồi ngược không được lệch nhau hơn 2°C. | Tm của probe cao hơn mồi 8-10℃ |
| Cấu trúc thứ cấp | Hạn chế hình thành cấu trúc thứ cấp ΔG > -9kcalo/mol | |
| Độ đặc hiệu | Khả năng bắt cặp chuyên biệt lên trình tự mục tiêu quan tâm | |
Các phần mềm hỗ trợ thiết kế mồi và đầu dò
Thiết kế mồi và đầu dò trong thực tế có thể thực hiện bằng cách thủ công, tuy nhiên việc này tốn nhiều thời gian thực hiện vì có nhiều thông số cần tính toán. Do đó, hiện nay có nhiều công cụ tin sinh học trực tuyến và thương mại được sử dụng thường xuyên để thiết kế mồi/đầu dò đặc hiệu, đạt hiệu quả khuếch đại qPCR, khả năng tái tạo và độ nhạy cao hơn.
Một số công cụ phân tích trình tự và thiết kế mồi phổ biến:
- Clustal: Sắp gióng cột các trình tự
- Annhyb: Phân tích trình tự
- Bioedit: Thiết kế mồi, phân tích trình tự
- Primer3 (Whitehead Institute, MIT)
- GeneFisher (Bielefeld University)
- FastPCR (PrimerDigital, Helsinki, Finland)
- PerlPrimer (Owen Marshall)
- Primer Design Assistant (Division of Biostatistics and Bioinformatics, NHRI)
- Beacon Designer (Premier Biosoft Intl)*
Công cụ kiểm tra độ đặc hiệu của mồi:
- Primer-Blast (NCBI)
Công cụ kiểm tra mồi:
- OligoAnalyzer (IDT)
- NetPrimer (Premier Biosoft)
- Oligonucleotide Properties Calculator (Northwestern University)
Thiết kế tối ưu các đoạn mồi và đầu dò cho real-time PCR bằng một số công cụ trên là điều cần thiết để đảm bảo khuếch đại hiệu quả và đặc hiệu các sản phẩm khuếch đại. Người sử dụng cần kiểm tra kỹ lưỡng các ưu điểm và nhược điểm của phần mềm trước khi lựa chọn, đặc biệt tránh các đoạn mồi có cấu trúc thứ cấp.
Dưới đây là một bảng so sánh các công cụ thiết kế mồi và phân tích oligonucleotide với các phần mềm thiết kế và phân tích mồi trực tuyến phổ biến khác do công ty cung cấp phần mềm jPCR Tool &FastPCR thống kê.
| Đặc điểm | FastPCR | NCBI/Primer-BLAST (Primer3) | BatchPrimer3 (Primer3) | IDT SciTools: PrimerQuest, OligoAnalyzer 3.1 | PerlPrimer | BiSearch Web server | Primo Pro 3.4 |
| Độ dài mồi/đầu dò (nt) | 12-500 | 15-30 | 16-35 | 12-30 | 10-35 | 13-36 | |
| Giới hạn độ dài khuôn mẫu (nt) | Không giới hạn | 50,000 | Không giới hạn | Không giới hạn | 5000 | Không giới hạn | |
| Tốc độ tính toán | Rất nhanh | Chậm | Chậm | Chậm | Chậm | Rất chậm | Nhanh |
| Cho phép chạy thông lượng cao với nhiều mẫu và nhiều mục tiêu trên khuôn cùng lúc | Có | Không | Có | Không | Không | Không | Có |
| Tùy chọn PCR cho khuôn mẫu | Có | Có | Có | Có | Có | Có | Có |
| Các nucleotide thoái hóa (tính toán Tm, tìm kiếm và thiết kế mồi, v.v.) | Có | Không | Có | Có | Không | Có | Không |
| Biến đổi LNA và nucleotide khác | Có | Không | Không | Có | Không | Không | Không |
| Hiệu quả PCR mồi và xác định tính phức tạp. | Có, LC=91.1±3.6% (6000 primers) | Không, LC=79.6±9.4% (6000 primers) | Không | Không, LC=84.4±8.1% (407 primers) | Không | Không, LC=73.2±10.8% (524 primers) | Không |
| Tính toán nhiệt độ ủ tối ưu | Có | Không | Không | Không | Không | Không | Không |
| Kiểm tra đầu 3′ của Primer và tự tạo dimer | Có | Lỗi | Có | Có | Có | Có | Có |
| Kiểm tra mồi nội giao và tự tạp dimer | Có | Lỗi | Không | Lỗi | Có | Có | Không |
| Tìm kiếm khuôn mẫu Blast | Không | Có | Không | Không | Có | Có | Có |
| Các thông số thiết kế mồi được đánh giá trong phòng thí nghiệm | Có | Có | Có | Có | Có | Có | Có |
*Các thông số so sánh chỉ mang giá trị tham khảo.
Sau khi mồi và đầu dò được thiết kế thành công cần kiểm tra tính đặc hiệu và khả năng khuếch đại bằng cách kiểm tra in silico và PCR thực nghiệm.
Trình tự mồi/đầu dò sau khi thiết kế được gửi đến các công ty dịch vụ tổng hợp oligonucleotide để tiến hành tổng hợp chuẩn bị cho các thí nghiệm. Hiện nay, OligoX là thương hiệu thuộc công ty TNHH GIẢI PHÁP Y SINH ABT phát triển cung cấp các loại mồi/đầu dò tổng hợp chất lượng cao, đáp ứng đầy đủ các yêu cầu của khách hàng trong nhiều lĩnh vực ứng dụng khác nhau, từ nghiên cứu khoa học đến ứng dụng y tế và công nghệ.
Tài liệu kham khảo
- Basu, Chhandak. (2015). [Methods in Molecular Biology] PCR Primer Design Volume 1275 || Design of Primers and Probes for Quantitative Real-Time PCR Methods. , 10.1007/978-1-4939-2365-6(Chapter 3), 31–56. doi:10.1007/978-1-4939-2365-6_3
- Juntaek Lim; Seung Gu Shin; Seungyong Lee; Seokhwan Hwang. (2011). Design and use of group-specific primers and probes for real-time quantitative PCR. , 5(1), 28–39. doi:10.1007/s11783-011-0302-x
- PrimerDigital, Online PCR primer software comparision (primerdigital.com)
- qPCR Assay Design and Optimization | Bio-Rad
- Sinh học Việt Nam, (2018), Thiết kế mồi cho phản ứng PCR

