1. Kỹ thuật Real-time PCR
Việc phát minh ra phản ứng chuỗi polymerase (PCR) của Kary Mullis vào năm 1984 được coi là một cuộc cách mạng trong khoa học. Tuy nhiên PCR cơ bản chỉ dừng lại ở việc khuếch đại trình tự DNA, điều đó là chưa đủ cho việc đáp ứng các nhu cầu ngày càng đa dạng trong nghiên cứu và ứng dụng sinh học phân tử. Kỹ thuật real-time PCR hay quantitative PCR (viết tắt là qPCR) là một trong những cải tiến PCR cơ bản, cụ thể ngoài khuếch đại trình tự mục tiêu kỹ thuật này còn định lượng được có bao nhiêu DNA mục tiêu trong mẫu nhờ vào tín hiệu huỳnh quang phát ra được máy ghi lại trong quá trình diễn ra phản ứng.
Real-time PCR là kỹ thuật cải tiến từ PCR, cho phép theo dõi sự gia tăng và định lượng DNA mục tiêu trong mẫu thử trong suốt thời gian thực tế diễn ra phản ứng nhờ vào công nghệ phát huỳnh quang.
2. Nguyên tắc của kỹ thuật Real-time PCR
Kỹ thuật real-time PCR về cơ bản vẫn là PCR, do vậy nguyên tắc vẫn là dùng cặp mồi đặc hiệu để phát hiện và khuếch đại trình tự mục tiêu bằng cách thay đổi nhiệt độ theo chu kỳ. Điểm khác biệt đó là real-time PCR còn dựa trên nguyên tắc sử dụng các mẫu dò hay thuốc nhuộm phát huỳnh quang để chỉ thị sự gia tăng bản sao trình tự mục tiêu, lượng tín hiệu ghi nhận được đo bằng máy trong thời gian thực hiện phản ứng.
Khi phản ứng nhân bản xảy ra tới một chu kỳ nhất định, cường độ tín hiệu huỳnh quang sẽ bắt đầu có sự gia tăng rõ rệt và tương quan với số lượng bản sao DNA được tạo ra. Kết quả được thể hiện trên máy tính dưới dạng biểu đồ quan sát được qua mỗi chu kỳ, từ đó có thể đưa ra đánh giá về hiệu quả khuếch đại DNA mục tiêu. Real-time PCR yêu cầu có thiết bị đo cường độ phát huỳnh quang từ ống mẫu và cài chương trình phần mềm cho phép xử lý kết quả về sự biến đổi cường độ huỳnh quang.
3. Chu trình Real-time PCR
Về cơ bản, phản ứng real-time PCR cũng tương tự PCR, bao gồm nhiều chu kỳ luân nhiệt nối tiếp nhau (30-45 chu kỳ), mỗi chu kỳ bao gồm ba bước chính:
Bước 1: Giai đoạn biến tính (Denaturation)
Nhiệt độ sẽ được đưa lên 94 – 95 oC trong khoảng 5 – 30 giây, lúc này các liên kết hydro bị phá vỡ và sợi đôi DNA bị biến tính thành hai sợi đơn.
Bước 2: Giai đoạn bắt cặp (Annealing) và kéo dài
Nhiệt độ được hạ xuống phù hợp cho các đoạn mồi bắt cặp bổ sung vào hai đầu trình tự mục tiêu (thường khoảng 55 – 65 oC). Ở bước này, ngay sau khi mồi gắn vào sợi khuôn, DNA polymerase sẽ ngay lập tức nhận biết vị trí và bắt đầu sử dụng dNTP tự do để kéo dài đầu 3′-OH của mồi.
Bước 3: Giai đoạn kéo dài bổ sung (Extension)
Ở bước này, nhiệt độ được đưa lên 72 oC để tối ưu cho hoạt tính tổng hợp của DNA polymerase, lúc này thời gian phản ứng sẽ tùy thuộc vào độ dài mục tiêu, thường khoảng 30 giây cho đến vài phút.
Như vậy, sau mỗi chu kỳ gồm ba bước lặp đi lặp lại, số lượng bản sao DNA mục tiêu sẽ gia tăng theo cấp số nhân (2n bản sao, với n là số chu kỳ). Điểm khác với PCR đó là việc định lượng DNA mục tiêu được thực hiện trong giai đoạn bản sao tăng lên theo cấp số nhân. Qua mỗi chu kỳ, lượng tín hiệu huỳnh quang tăng lên sẽ được ghi nhận tương ứng với lượng bản sao DNA được tạo ra. Bên cạnh đó, kỹ thuật real-time PCR thường được ứng dụng vào mục đích xét nghiệm bệnh, do đó phải đáp ứng yêu cầu kết quả chính xác và nhanh chóng.
Do vậy, Real-time PCR dùng trong xét nghiệm thường chỉ bao gồm hai bước biến tính và bắt cặp là đủ để khuếch đại các trình tự mục tiêu có độ dài <200 bp. Điều này giúp tiết kiệm thời gian, nhanh chóng phát hiện và định lượng được DNA mục tiêu trong chẩn đoán sinh học phân tử.
4. Cơ chế phát huỳnh quang
Dựa trên cơ chế liên kết và phát huỳnh quang, real-time PCR có thể phân loại các phân tử phát huỳnh quang thành hai nhóm chính. Nhóm thứ nhất bao gồm các phân tử phát huỳnh quang gắn chèn vào DNA sợi đôi, trong khi nhóm thứ hai bao gồm các phân tử probe được đánh dấu huỳnh quang có khả năng liên kết đặc hiệu với sản phẩm PCR được tạo ra.
Các chất phát huỳnh quang gắn chèn vào DNA sợi đôi là những chất này thường phát ra ánh sáng huỳnh quang với cường độ cao hơn nhiều khi được liên kết với DNA (Hình 1). Khi chúng kết hợp với DNA, tạo thành một hợp chất phát quang có khả năng phát ra ánh sáng với cường độ cao hơn nhiều so với khi ở dạng tự do, khi bị kích thích bởi ánh sáng hoặc tia UV. Điều này cho phép quan sát và đo lường sự hiện diện và lượng DNA trong mẫu.
Cường độ của tín hiệu huỳnh quang tăng theo tỷ lệ với lượng DNA có mặt trong mẫu, điều này cho phép xác định định lượng DNA một cách chính xác và đáng tin cậy. Các chất phát huỳnh quang này khi ở dạng tự do vẫn phát ra ánh sáng với cường độ thấp khi bị kích thích, tạo ra tín hiệu nền trong phản ứng real-time PCR. Một số chất huỳnh quang phổ biến được dùng trong real-time như SYBR Green, EvaGreen, LC Green, SYTO9, …
(https://app.biorender.com)
Còn probe đánh dấu huỳnh quang là các oligonucleotide được thiết kế để phát ra tín hiệu huỳnh quang khi liên kết với đoạn sản phẩm PCR mục tiêu. Các loại probe như TaqMan probes, molecular beacons và Scorpion probes có khả năng phát ra ánh sáng khi được thủy giải trong quá trình PCR. Công nghệ Taqman probe được sử dụng rộng rãi trong lĩnh vực xét nghiệm.
Taqman probe là đoạn oligonucleotide sợi đơn có thể bắt cặp đặc hiệu với một đoạn trình tự trên DNA mục tiêu, bao gồm đầu 5’ gắn chất phát huỳnh quang (reporter) và đầu 3’ gắn chất hấp phụ huỳnh quang (quencher). Khi cấu trúc của mẫu dò còn nguyên vẹn thì đầu quencher sẽ làm tắt tín hiệu huỳnh quang phát ra từ đầu reporter nếu khoảng cách hai đầu này đủ gần bởi cơ chế FRET (fluorescence resonance energy transfer – truyền năng lượng cộng hưởng). Khi có sự hiện diện của DNA mục tiêu, phản ứng PCR xảy ra và trong quá trình kéo dài, Taq polymerase gặp TaqMan probe sẽ dừng lại và bắt đầu nén, đồng thời hoạt tính 5’-3’ exonuclease thủy giải Taqman probe. Khi TaqMan probe bị thủy giải, reporter được giải phóng khỏi quencher, tạo ra tín hiệu huỳnh quang khi có ánh sáng kích thích. Cường độ tín hiệu huỳnh quang sẽ tăng lên sau mỗi chu kỳ, tương ứng với sự tăng lên của sản phẩm PCR (Hình 2).

(https://app.biorender.com)
5. Các khái niệm cơ bản trong Real-time PCR
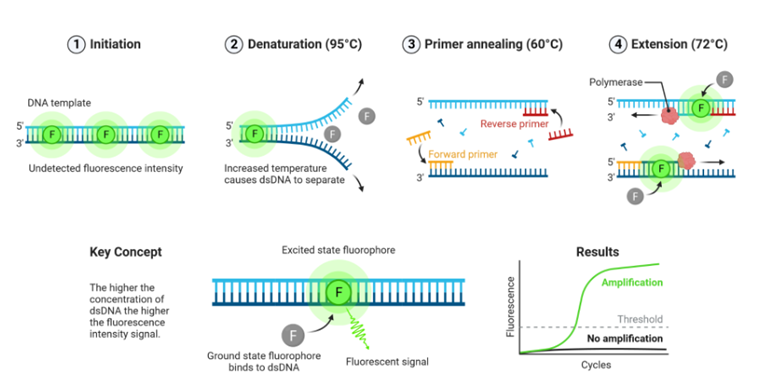
Trong quá trình phản ứng Real-time PCR xảy ra, cường độ tín hiệu huỳnh quang thu nhận được sẽ chuyển đổi thành dạng biểu đồ đường, biểu đồ này sẽ bao gồm các thông số về tín hiệu nền (background), đường nền (baseline) và chu kỳ ngưỡng (cycle threshold – Ct) (Hình 3) chi tiết được trình bày như sau:
– Tín hiệu nền (Background): là các tín hiệu huỳnh quang nền được tạo thành không liên quan đến phản ứng real-time PCR. Tín hiệu này thường do đầu reporter của probe phát ra, về lý thuyết thì ở điều kiện bình thường quencher sẽ hấp thụ hết tín hiệu do reporter phát ra, nhưng thực tế quencher không thể hấp thụ 100% tín hiệu do reporter phát ra nên trong hầu hết các phản ứng real-time PCR đều xuất hiện tín hiệu nền. Ngoài ra, mỗi loại probe khác nhau, nhà sản xuất khác nhau thì tín hiệu nền của từng probe sẽ khác nhau. Ngày nay, các hãng tổng hợp probe cũng đã thiết kế ra nhiều cách để hạn chế tín hiệu nền này như dual quencher, …Về trường hợp sử dụng SYBR Green, ban đầu khi chưa có trình tự mục tiêu thì chất này vẫn phát huỳnh quang trong dung dịch tuy nhiên do phân tán đều trong dung dịch nên cường độ sẽ yếu và tạo thành tín hiệu nền cho phản ứng. Những chu kỳ đầu của real-time, nồng độ ban đầu của mẫu thấp nên cường độ huỳnh quang phát ra không đủ để máy real-time PCR có thể ghi nhận được và giai đoạn này thường chỉ ghi nhận được tín hiệu nền của mẫu.
– Đường nền (Baseline): là đường biểu diễn mức độ tín hiệu trong suốt những chu kỳ đầu của real-time PCR. Việc thiết lập baseline là bước quan trọng trong phân tích kết quả real-time PCR do baseline không cố định (có thể điều chỉnh), giá trị baseline sẽ ảnh hưởng nhiều tới việc xác nhận tính chất của mẫu. Nếu điều chỉnh giá trị baseline quá thấp, kết quả sẽ rất dễ thu nhận tín hiệu nhiễu (dương tính giả), ngược lại giá trị baseline quá cao, kết quả sẽ có độ chính xác thấp vì bỏ qua các mẫu dương yếu (âm tính giả). Vì vậy, giá trị baseline nên được điều chỉnh khoảng 5% so với giá trị tín hiệu huỳnh quang cao nhất của mẫu (theo khuyến cáo của hãng).
– Ngưỡng (Threshold): là mức tín hiệu mà ở đó nó phản ánh sự gia tăng tín hiệu có ý nghĩa về mặt thống kê, giúp phân biệt tín hiệu khuếch đại vượt qua khỏi tín hiệu nền. Thông thường giá trị ngưỡng được thiết lập dựa vào đường nền hoặc mức tín hiệu thực tế của mẫu. Cách thiết lập giá trị ngưỡng tương tự như baseline.
– Chu kỳ ngưỡng (Ct – threshold cycle): là số chu kỳ mà tại điểm đó tín hiệu huỳnh quang của phản ứng vượt lên cắt đường ngưỡng, thay đổi từ âm tính (không thể phát hiện được) sang dương tính (có thể phát hiện được). Giá trị chu kỳ ngưỡng (Ct) phản ánh lượng gene quan tâm trong giai đoạn đầu của phản ứng và tỷ lệ nghịch với mức biểu hiện tương đối ban đầu của gene quan tâm. Nếu giá trị Ct càng nhỏ có nghĩa là nồng độ gene quan tâm ban đầu càng lớn và ngược lại.
– Passive reference dyes: thường được sử dụng trong real-time PCR để chuẩn hóa tín hiệu huỳnh quang của Reporter và hiệu chỉnh sự dao động về tín hiệu huỳnh quang không tạo thành do phản ứng PCR giữa các giếng. Không phải máy nào cũng có chế độ này do vậy cần xem kỹ thông tin của máy để chọn loại hóa chất sao cho phù hợp.
(https://geneeticeducation.co.in)
6. Phân tích kết quả Real-time PCR
Ngoài việc giống với kết quả PCR giúp định tính tác nhân mục tiêu, xét nghiệm qPCR còn được bổ sung thêm chức năng xác định chính xác số lượng DNA mục tiêu có trong mẫu. Kỹ thuật này yêu cầu xây dựng đường chuẩn dựa vào giá trị Ct và dãy nồng độ DNA đã biết trước. Nồng độ DNA mục tiêu sẽ được xác định thông qua đường chuẩn, do vậy các thông số đường chuẩn phải đạt yêu cầu để phản ánh độ tin cậy cũng như chất lượng kết quả xét nghiệm của qPCR định lượng.
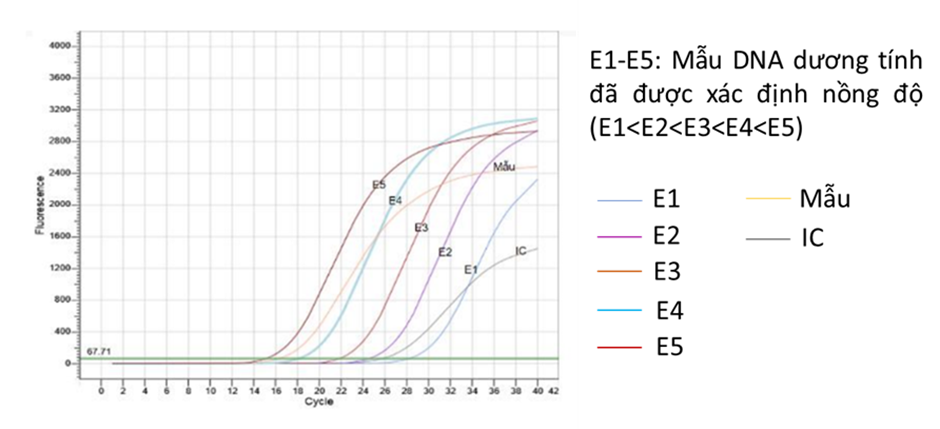
Theo định nghĩa, đường chuẩn được xây dựng từ giá trị chu kỳ ngưỡng (Ct) của một dãy các ống chứa DNA có nồng độ tuyến tính đã được xác định trước (thường pha loãng theo bậc 10 như 101, 102, 103, …) (Hình 4). Nồng độ được chọn cho việc xây dựng đường chuẩn phải bao quát được nồng độ dự kiến của DNA mục tiêu có trong mẫu thử nghiệm. Đường chuẩn bao gồm trục x (giá trị nồng độ chuẩn) và trục y (giá trị Ct). Các thông số của đường chuẩn như hệ số tuyến tính (R2), hiệu suất khuếch đại (E%) và độ dốc (slope) được máy tính toán dựa trên kết quả ghi nhận thực tế, giúp xác định chất lượng của một phản ứng qPCR, cụ thể:
– Hệ số tuyến tính (R2): phản ánh mức độ tuyến tính của các giá trị trong đường chuẩn, R2 lý tưởng là tiến đến 1, thực tế giá trị tối đa chỉ tới mức 0,999.
– Hiệu suất khuếch đại (E%): phản ánh mức độ hiệu quả của phản ứng khuếch đại. E% lý tưởng là 100%, đó là khi DNA mục tiêu tăng gấp đôi sau mỗi chu kỳ nhiệt trong giai đoạn lũy thừa của phản ứng. Tuy nhiên trên thực tế, hiệu quả khuếch đại sẽ có sự sai lệch so với giá trị lý tưởng, cụ thể dao động trong khoảng 90 – 110%. Nếu E thấp, nguyên do có thể là độ nhạy của mồi chưa cao hay phản ứng bị ức chế, nếu E cao có thể là mồi bắt cặp đặc hiệu. Một số yếu tố về thành phần như chiều dài gene đích, thành phần GC, các cấu trúc thứ cấp hình thành hay thao tác người thực hiện sẽ ảnh hưởng đến E%. Trong nghiên cứu, thao tác pha loãng mẫu chuẩn cũng sẽ ảnh hưởng đến hiệu suất. Ví dụ, khi pha loãng mẫu chuẩn từ nồng độ cao đến thấp sẽ dễ gặp phải trường hợp thể tích mẫu nồng độ cao trước đó sẽ còn dính ở đầu tip dẫn đến lượng DNA thực tế ở các ống pha loãng sau đó sẽ cao hơn dự kiến, do vậy E có thể cao hơn 100%. Trường hợp ngược lại nếu khi dung dịch không được đẩy ra hết cũng làm giảm giá trị E.
– Độ dốc (slope): được coi là thước đo hiệu suất khuếch đại. Nói cách khác đường chuẩn được xây dựng với các mẫu chuẩn nếu cách nhau qua độ pha loãng hệ số 10 thì hiệu quả khuếch đại E được tính theo công thức 10-1/slope với slope chính là độ đốc của đường biểu diễn chuẩn. Với hiệu quả lý tưởng là sản phẩm bản sao tăng lên gấp đôi so với khuôn ban đầu thì 10-1/slope = 2, như vậy slope lý tưởng là -3,32 tương đương E=100%. Tuy nhiên, thực tế khó có thể đạt được điều kiện như vậy, do đó slope thường dao động trong khoảng từ -3,58 đến -3,10.
Sau phản ứng, dựa vào phương trình y=ax+b của đường chuẩn sẽ giúp xác định được nồng độ DNA mục tiêu có trong mẫu (Hình 34). Như vậy đường chuẩn là một thông số để xác định hàm lượng bản sao DNA có trong mẫu và đánh giá hiệu quả của phản ứng khuếch đại. Hiện nay, trên thị trường một số kit qPCR đã cung cấp sẵn các ống nồng độ chuẩn để đảm bảo việc xây dựng đường chuẩn chính xác, không bị ảnh hưởng nhiều bởi thao tác người thực hiện.
7. Phân tích kết quả định lượng HBV
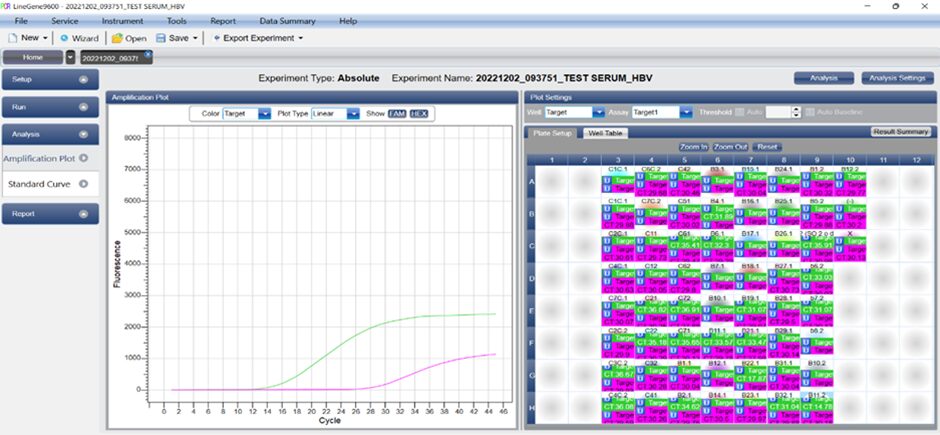
Xét nghiệm: xác định sự hiện diện và định lượng tác nhân HBV trong mẫu huyết thanh bằng bộ kit ABT® DNA QUANTITATIVE PCR KIT (SQH-001) bằng hệ thống Real-time PCR LineGene 9600.
7.1. Phân tích định tính
Phân tích kết quả của từng mẫu (xác định mẫu dương tính, âm tính hay không xác định được kết quả)
– Có tín hiệu huỳnh quang được phát hiện ở kênh màu FAM => Mẫu dương tính: mẫu chứa HBV-DNA. Trong trường hợp này, tín hiệu ở kênh màu HEX có thể bình thường hoặc thấp vì khi nồng độ HBV-DNA cao (tín hiệu dương tính ở kênh màu FAM) có thể dẫn đến việc giảm hoặc không có tín hiệu huỳnh quang của đối chứng nội trong kênh màu HEX (cạnh tranh).
– Ở kênh màu FAM không có tín hiệu được phát hiện và có tín hiệu của đối chứng nội ở kênh màu HEX. Trong mẫu không có HBV-DNA được phát hiện: mẫu được xem là âm tính.
– Không có tín hiệu được phát hiện ở cả kênh màu FAM và HEX: không thể kết luận kết quả.
Phân tích kết quả của một số trường hợp thực tế
– Trường hợp 1: Kết quả HBV dương tính vì tín hiệu huỳnh quang được phát hiện ở kênh màu FAM và HEX.
– Trường hợp 2: Kết quả HBV âm tính vì tín hiệu huỳnh quang chỉ phát hiện ở kênh màu HEX mà không phát hiện ở kênh màu FAM.
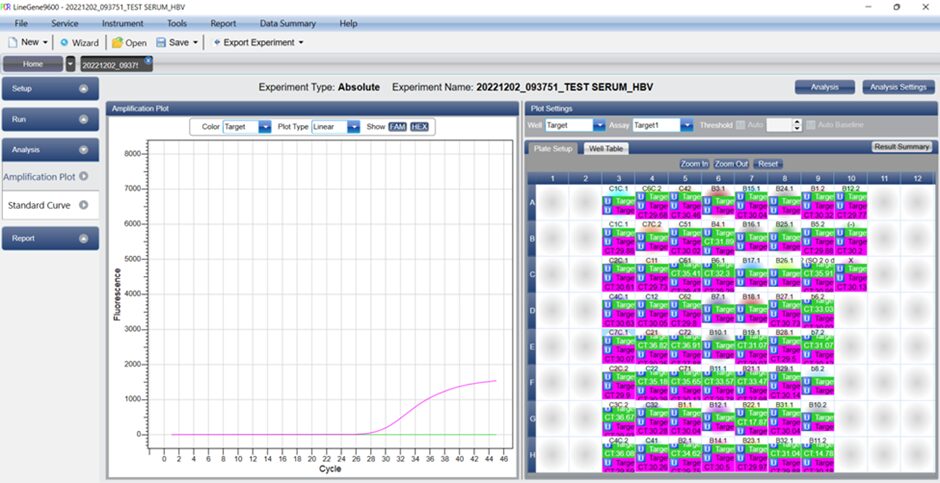
7.2. Phân tích định lượng
Phân tích kết quả đường chuẩn:
– Giá trị Correlation phản ánh độ tuyến tính của đường chuẩn. Lý tưởng nhất là Correlation = 1, mặc dù 0,999 thường là giá trị tối đa đạt được.
– Efficiency (E) của phản ứng PCR phải là 100% nghĩa là mẫu tăng gấp đôi sau mỗi chu kỳ nhiệt trong quá trình khuếch đại hàm mũ. Một phản ứng tốt sẽ có giá trị của E từ 90% đến 110%.
– Slope (độ dốc) là thước đo hiệu suất phản ứng. Để có được kết quả chính xác và có tính lặp lại, các phản ứng nên có hiệu quả càng gần 100% càng tốt, tương đương với slope (độ dốc) càng gần -3,32.
Nhập kết quả ghi nhận từ phần mềm vào File Dữ liệu
– Nồng độ của HBV ở các mẫu dương tính được tính toán theo Hướng dẫn sử dụng của bộ kit định lượng HBV ABT® DNA QUANTITATIVE PCR KIT (SQH-001)
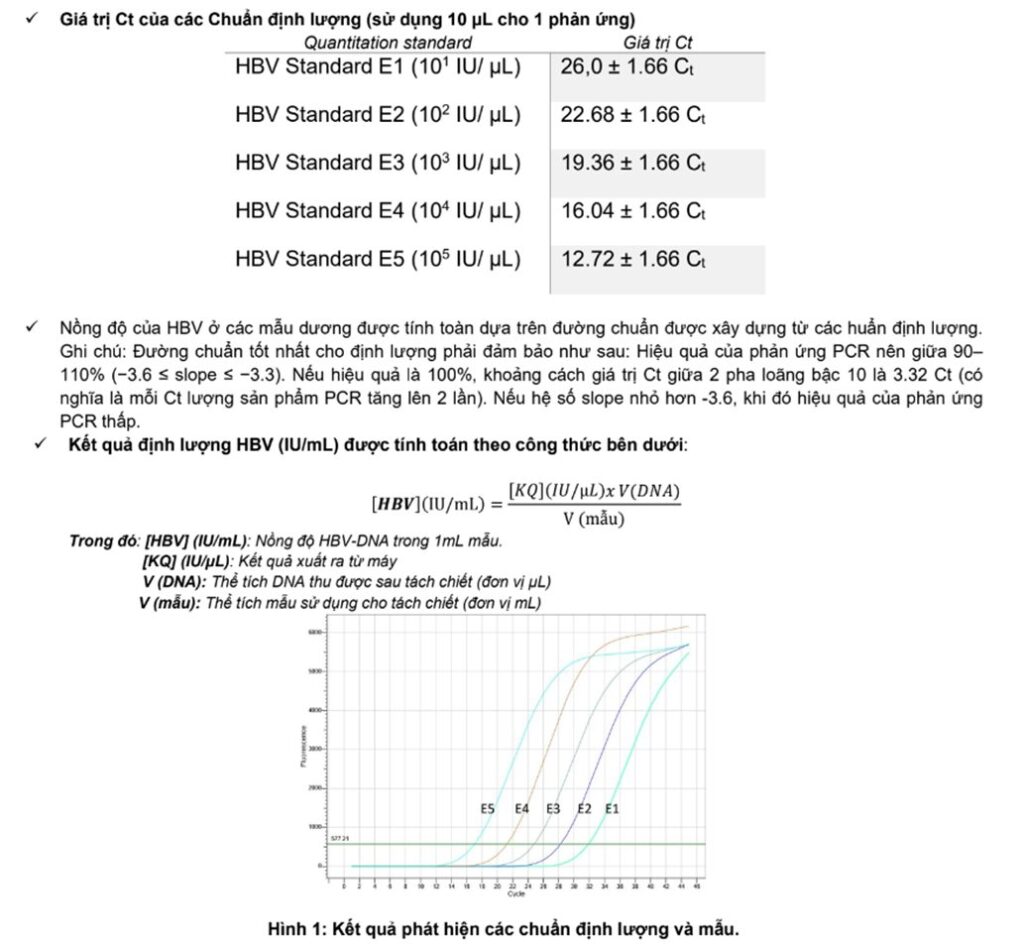
Đường chuẩn HBV:
Để tạo đường chuẩn trên thiết bị Real-time PCR, tất cả 5 mẫu chuẩn định lượng nên được sử dụng và được nhập vào máy ở chế độ “standard” với các nồng độ đã biết (Hình 8).
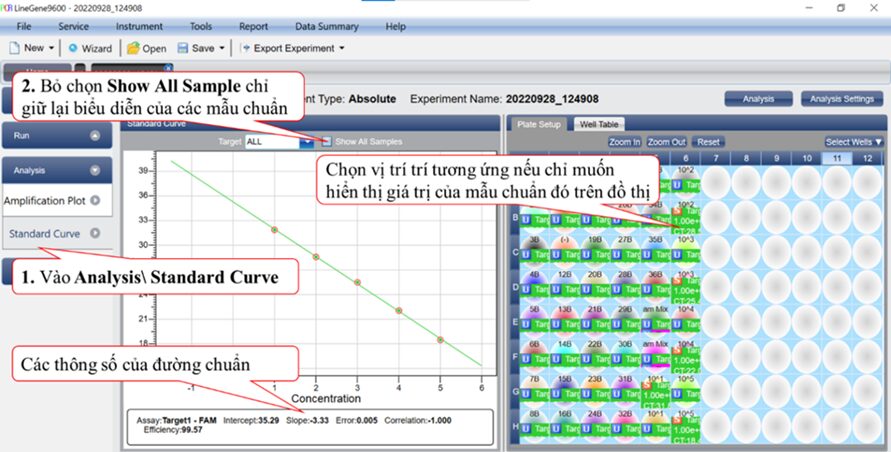
Sau khi dựng đường chuẩn bằng phần mềm đi kèm với máy thì tiến hành đọc kết quả mẫu được xuất ra file excel (Hình 9).
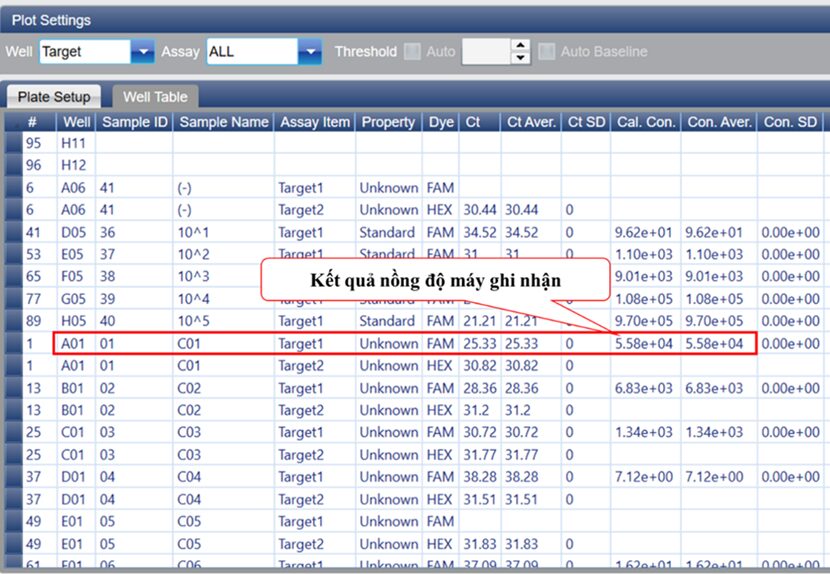
Với 0,2 mL mẫu huyết thanh sau khi tách chiết nucleic acid tinh sạch được hòa trong dung dịch rửa giải thu được thể tích 50 μL, sau khi thực hiện phản ứng qPCR một bước kết quả nồng độ ghi nhận từ máy là 5,58 × 10⁴ (5.58e+4) (IU/µL) (Hình 9), áp dụng công thức:
[HBV](IU/mL) = (5,58.104 (IU/μL) x 50 (μL))/0,2 mL = 1,4 × 10⁷ (IU/mL)
Kết luận, bộ kit ABT® DNA Quantitative PCR được sử dụng để phát hiện định lượng sự hiện diện của DNA-HBV có trong mẫu huyết thanh/huyết tương bằng kỹ thuật real-time PCR, với độ nhạy phân tích đạt 28 IU/mL.
8. Tài liệu tham khảo
1. Higuchi, R., Fockler, C., Dollinger, G., & Watson, R. (1993). Kinetic PCR analysis: real-time monitoring of DNA amplification reactions. Bio/technology, 11(9), 1026-1030.
2. Bustin, S. A. (2002). Quantification of mRNA using real-time reverse transcription PCR (RT-PCR): trends and problems. Journal of molecular endocrinology, 29(1), 23-39.
3. Ponchel, F., Toomes, C., Bransfield, K., Leong, F. T., Douglas, S. H., Field, S. L., … & Markham, A. F. (2003). Real-time PCR based on SYBR-Green I fluorescence: an alternative to the TaqMan assay for a relative quantification of gene rearrangements, gene amplifications and micro gene deletions. BMC biotechnology, 3, 1-13.

