Ở bài viết trước, chúng ta đã tìm hiểu tổng quan về PCR kỹ thuật số dPCR và hướng dẫn thực hiện trên hai hệ thống phổ biến là Bioer (cdPCR) và Bio-Rad (ddPCR). Bài viết này sẽ đi sâu vào tìm hiểu ứng dụng PCR kỹ thuật số vi giọt (Droplet Digital PCR hay ddPCR) như một công cụ chẩn đoán đầy tiềm năng cho bệnh nhân ung thư phổi không tế bào nhỏ (non-small cell lung cancer).
1. Ung thư phổi không tế bào nhỏ (NSCLC) là gì?
Ung thư phổi là loại ung thư được chẩn đoán nhiều thứ hai trên thế giới, chỉ sau ung thư vú. Tại Việt Nam, ung thư phổi nằm trong nhóm ba loại ung thư thường gặp nhất (GLOBOCAN, 2022), tỷ lệ sống sót ở giai đoạn cuối thường thấp. Dựa trên hình thái tế bào và miễn dịch học, ung thư phổi được chia thành ung thư phổi tế bào nhỏ (10-15%) và ung thư phổi không tế bào nhỏ (NSCLC) (Hình 1).
Ung thư phổi không tế bào nhỏ (NSCLC) là loại ung thư phổ biến nhất, chiếm khoảng 85-90% các trường hợp. Đây là một nhóm các loại ung thư phổi có đặc điểm tế bào lớn hơn và phát triển chậm hơn so với ung thư phổi tế bào nhỏ. NSCLC được phân loại thành ung thư biểu mô tế bào tuyến (40% của NSCLC), ung thư biểu mô tế bào lớn (10-15% của NSCLC), ung thư biểu mô tế bào vảy (25-30% của NSCLC) và khối u carcinoid phế quản.
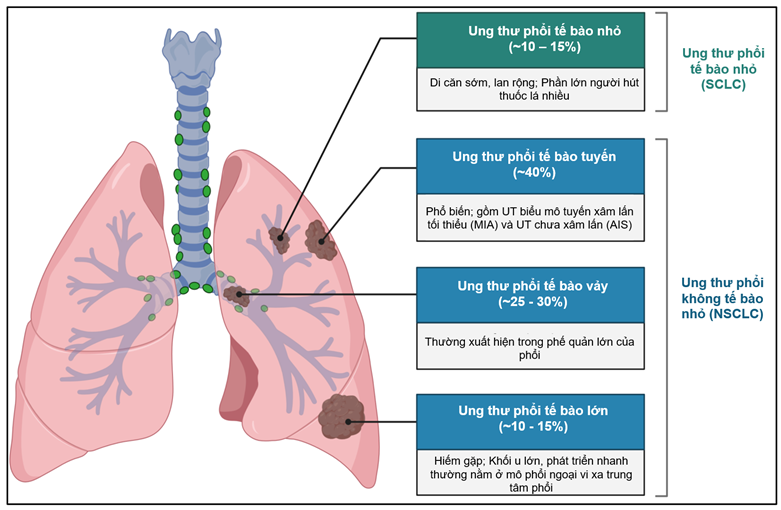
Nguyên nhân gây ung thư phổi không tế bào nhỏ được xác định do nhiều yếu tố nguy cơ. Ước tính 80-90% ung thư phổi liên quan đến thuốc lá. Một người hút một gói thuốc mỗi ngày có nguy cơ mắc ung thư phổi gấp 20 lần người không hút thuốc. Người sống cùng nhà với người hút thuốc tăng 30% nguy cơ ung thư phổi so với người không cùng hoàn cảnh. Một số yếu tố khác do tiếp xúc amian, bụi phóng xạ và radon, nhiễm khuẩn, ô nhiễm không khí và các bệnh di truyền.
Theo hướng dẫn của Mạng lưới Ung thư Toàn diện Quốc gia Hoa Kỳ (National Comprehensive Cancer Network), các đột biến hoặc biến đổi gene trong NSCLC thường không trùng lặp, nhưng 1–3% trường hợp có thể mang đồng thời nhiều đột biến. Các đột biến chủ yếu bao gồm EGFR, EGFR p.T790M, EGFRex20, ALK, ROS1, BRAF, KRAS, MET, RET, ERBB2, HER2, NTRK1/2/3, PD-L1. Trong đó, đột biến gene chiếm tỷ lệ cao là EGFR (35.4%) và KRAS (22.6%). Nhiều đột biến gene ảnh hưởng đến lựa chọn phương pháp điều trị, do đó cần xét nghiệm các dấu ấn sinh học từ mô hoặc máu để xác định liệu pháp nhắm trúng đích phù hợp, tránh các phương pháp kém hiệu quả. Năm 2021, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ FDA đã chấp thuận sotorasib và amivantamab điều trị các khối u chứa KRAS G12C và đột biến chèn thêm đoạn 20 exon vào gene EGFR. Tuy nhiên, bệnh nhân trước khi được chỉ định dùng thuốc ức chế EGFR cần phải được làm xét nghiệm tình trạng gene.
2. Các phương pháp chẩn đoán phân tử phát hiện ung thư phổi không tế bào nhỏ (NSCLC)
Tỷ lệ tử vong do ung thư phổi cao do bệnh thường được chẩn đoán vào giai đoạn tiến xa nên cần tăng cường hiệu quả hoạt động tầm soát, phát hiện sớm ung thư phổi. Mỗi phương pháp chẩn đoán bệnh đều có ưu và nhược điểm riêng, đòi hỏi bác sĩ lâm sàng phải cân nhắc kỹ trước khi lựa chọn phương pháp nhằm tiết kiệm thời gian, chi phí xét nghiệm và giảm bớt khó chịu cho bệnh nhân.
Phương pháp Real-time PCR được sử dụng phổ biến để xác định đột biến EGFR nhắm mục tiêu vào đột biến cụ thể. Giải trình tự thế hệ mới NGS giúp xác định toàn diện các biến đổi gene. Phương pháp lai huỳnh quang tại chỗ (FISH) được sử dụng để phân tích số lượng bản sao, khuếch đại gene và các thay đổi về cấu trúc như sắp xếp lại gene. Tuy nhiên, mỗi phương pháp đều có hạn chế. Ví dụ, IHC phụ thuộc nhiều vào thao tác kỹ thuật viên; FISH yêu cầu mẫu FFPE chất lượng cao; còn NGS và MLPA có quy trình phức tạp, cần nhân sự chuyên môn cao và chi phí lớn
Gần đây, PCR kỹ thuật số vi giọt (ddPCR) đã được phát triển và ứng dụng rộng rãi trong phát hiện đột biến soma cũng như định lượng chính xác nucleic acid mục tiêu có trong mẫu. Một trong những ứng dụng quan trọng của ddPCR là khả năng định lượng nucleic acid tuyệt đối mà không cần sử dụng các đối chứng nội sinh. Phương pháp này có độ chính xác cao cho phép phát hiện một lượng nhỏ DNA đột biến, với tần số alen trong khoảng từ 0,001–0,4%. Nhờ độ nhạy vượt trội, ddPCR trở thành công cụ hữu ích để phát hiện đột biến hiếm có nguồn gốc từ các tế bào khối u trong một nền mẫu phức tạp.
3. Ứng dụng ddPCR trong nghiên cứu đột biến EGFR ở huyết tương của bệnh nhân ung thư phổi không tế bào nhỏ (NSCLC)
Trong ung thư phổi không tế bào nhỏ, thụ thể yếu tố tăng trưởng biểu bì (EGFR) là một glycoprotein xuyên màng biểu hiện mức độ cao ở các khối u phổi. Các đột biến EGFR phổ biến nhất nằm ở vùng tyrosine kinase của gene EGFR. Khi gene EGFR bị đột biến, tế bào có thể tăng sinh mất kiểm soát dẫn đến ung thư. Do đó, việc phát hiện đột biến EGFR đã trở thành đích nhắm cho liệu pháp điều trị đích, như thuốc ức chế tyrosine kinase (TKIs) điều trị hiệu quả NSCLC.
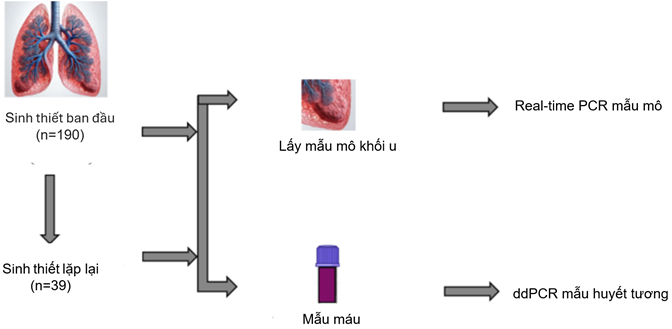
Ứng dụng kỹ thuật ddPCR, nhóm tác giả Lynn Yim-Wah Shong và cộng sự (2024) đã tiến hành xét nghiệm DNA huyết tương để phát hiện đột biến EGFR trong trường hợp mẫu mô khối u không đủ để phân tích. ctDNA (circulating tumor DNA) còn gọi là các đoạn DNA được giải phóng từ khối u vào máu của bệnh nhân ung thư. ctDNA mang đặc điểm di truyền đặc trưng của khối u, được sử dụng như một công cụ chẩn đoán phân tử không xâm lấn và theo dõi tiến triển khối u theo thời gian thực. Vì vậy, ctDNA trong huyết tương là mục tiêu phân tích kiểu gene để tìm đột biến EGFR bằng hệ thống PCR kỹ thuật số dạng giọt QX200 (Bio-Rad) theo quy trình đã trình bày ở bài viết trước. Đồng thời, các mẫu sinh thiết mô cũng được phân tích real-time PCR nhằm đánh giá tình trạng đột biến EGFR (Hình 2)
Trong số các bệnh nhân mới được chẩn đoán mắc ung thư phổi, các đột biến EGFR phổ biến được xác định trong mẫu huyết tương là L858R trên exon 21 và đột biến xóa đoạn exon 19. Đột biến EGFR hiếm gặp ở giai đoạn sớm (I và II) nhưng tỷ lệ phát hiện cao hơn đáng kể ở ung thư phổi giai đoạn IV, những phát hiện tương tự cũng được tìm thấy ở những bệnh nhân nghi ngờ ung thư phổi phản ánh mối liên hệ giữa lượng ctDNA huyết tương và mức độ tiến triển bệnh.
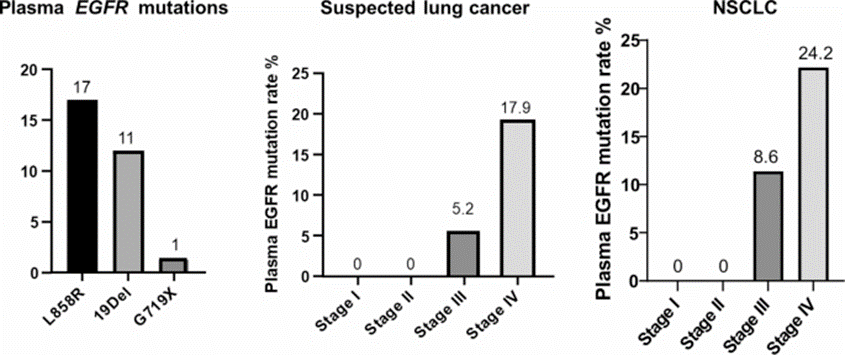
Xét nghiệm đột biến EGFR trong huyết tương bằng ddPCR là phương pháp không xâm lấn giúp phát hiện đột biến EGFR ở bệnh nhân nghi ngờ ung thư phổi tiến triển, đặc biệt đối với khối u khó tiếp cận hoặc khả năng không thu được mẫu mô chất lượng cao. Phương pháp này sử dụng mẫu máu hoặc huyết tương cho phép chẩn đoán hiệu quả các đột biến EGFR, góp phần hỗ trợ chẩn đoán và cải thiện tiên lượng bệnh.
Tuy nhiên, cũng cần lưu ý độ nhạy của ddPCR còn hạn chế trong việc phát hiện đột biến EGFR ở giai đoạn đầu. Vì vậy, cần phải nghiên cứu cải thiện hoặc có các chiến lược chẩn đoán kết hợp để nâng cao độ chính xác phát hiện ở giai đoạn đầu nhằm đưa ra quyết định lâm sàng chính xác cho bệnh nhân.
4. Tiềm năng ứng dụng ddPCR trong xét nghiệm ung thư phổi không tế bào nhỏ (NSCLC) tại Việt Nam
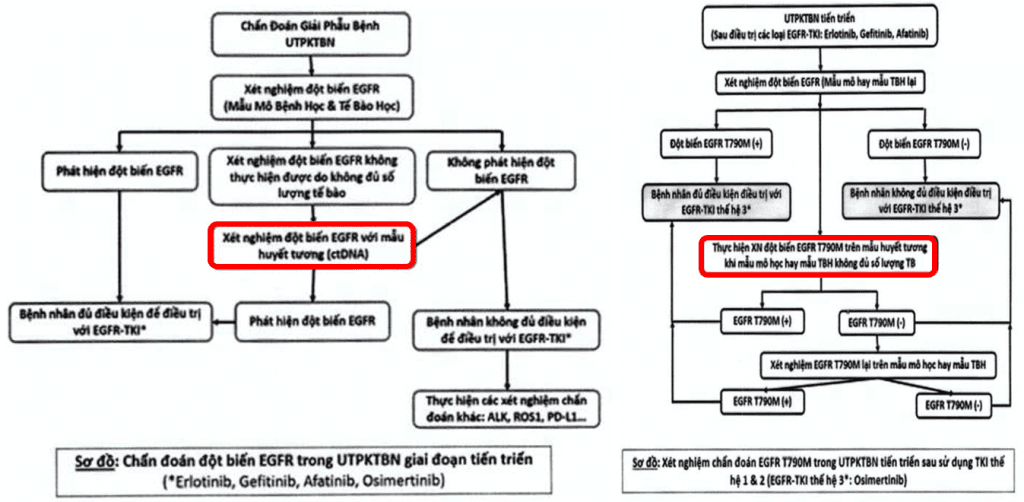
Theo quyết định Số 4825/QĐ-BYT ban hành tài liệu chuyên môn “hướng dẫn chẩn đoán và điều trị ung thư phổi không tế bào nhỏ”, PCR kỹ thuật số là một trong các phương pháp xét nghiệm sinh học phân tử được đề xuất sử dụng cho xét nghiệm chẩn đoán đột biến gene EGFR. Điển hình trong một số trường hợp mẫu mô bệnh học hay tế bào học không đủ số lượng để chẩn đoán sinh học phân tử, có thể dùng mẫu huyết tương để phát hiện các đột biến EGFR mắc phải hay thứ phát sau khi được điều trị các thuốc kháng tyrosine kinase (TKIs).
Ngoài ra, một số bệnh viện tại Việt Nam đã ứng dụng ddPCR trong xét nghiệm các đột biến gene khác liên quan đến nguy cơ ung thư, như đột biến gene BCR-ABL. Sau khi người bệnh được điều trị bằng thuốc đích, sẽ tiếp tục làm xét nghiệm để theo dõi quá trình điều trị giúp đánh giá số lượng bản sao của gene gây bệnh trong máu. Từ đó, đánh giá được tình trạng lui bệnh ở mức độ phân tử, giúp bác sĩ lâm sàng đưa ra quyết định ngưng thuốc cho người bệnh ở thời điểm thích hợp hoặc theo dõi, đánh giá hiệu quả cả quá trình điều trị và có thể tiên lượng khả năng tái phát của người bệnh theo thời gian, từ đó có thể đưa ra các phác đồ và hướng điều trị cho người bệnh.
Như vậy, hướng ứng dụng ddPCR vào xét nghiệm dấu ấn sinh học phân tử là một xu thế phát triển đầy tiềm năng trong tương lai. Phương pháp này không chỉ làm giảm bớt sự khó chịu cho bệnh nhân trong quá trình lấy mẫu mà còn gia tăng độ chính xác trong các xét nghiệm. Nhờ đó, bác sĩ có thể theo dõi hiệu quả điều trị, đánh giá tình trạng lui bệnh ở mức độ phân tử, tiên lượng khả năng tái phát và đưa ra các quyết định lâm sàng phù hợp, góp phần tối ưu hóa phác đồ điều trị cho người bệnh.
*Từ viết tắt:
ctDNA: DNA khối u lưu hành tuần hoàn
ddPCR: droplet digital PCR
dPCR: digital PCR
EGFR: thụ thể yếu tố tăng trưởng biểu bì
NCCN: Mạng lưới Ung thư Toàn diện Quốc gia
NSCLC: Ung thư phổi không tế bào nhỏ
UTPKTBN: Ung thư phổi không tế bào nhỏ
5. Tài liệu tham khảo
- Bộ Y tế. (2018). Quyết định số 4825/QĐ-BYT về việc ban hành tài liệu chuyên môn “Hướng dẫn chẩn đoán và điều trị ung thư phổi không tế bào nhỏ”. Cổng thông tin Thư viện Pháp luật. https://vnras.com/quyet-dinh-4825-qd-byt-2018/
- National Comprehensive Cancer Network. (2025). NCCN Clinical Practice Guidelines in Oncology: Non-Small Cell Lung Cancer (Version 8.2025). NCCN.org. https://www.nccn.org/professionals/physician_gls/pdf/nscl.pdf
- Nooreldeen, R., & Bach, H. (2021). Current and future development in lung cancer diagnosis. International Journal of Molecular Sciences, 22(8661). https://doi.org/10.3390/ijms22168661 Biên dịch: https://www.hoihohaptphcm.org/TaiLieu/CHAN%20DOAN%20UNG%20THU%20PHOI.pdf
- Oscorbin, I. P., Smertina, M. A., Pronyaeva, K. A., Voskoboev, M. E., Boyarskikh, U. A., Kechin, A. A., Demidova, I. A., & Filipenko, M. L. (2022). Multiplex Droplet Digital PCR Assay for Detection of MET and HER2 Genes Amplification in Non-Small Cell Lung Cancer. Cancers, 14(6), 1458. https://doi.org/10.3390/cancers14061458
- Shong, L.YW., Deng, JY., Kwok, HH. et al. Detection of EGFR mutations in patients with suspected lung cancer using paired tissue-plasma testing: a prospective comparative study with plasma ddPCR assay. Sci Rep 14, 25701 (2024). https://doi.org/10.1038/s41598-024-76890-0
- Yin, J., Xia, L., Zou, Z., Zhuang, J., & Mu, Y. (2022). A direct and multiplex digital PCR chip for EGFR mutation. Talanta, 250, 123725. https://doi.org/10.1016/j.talanta.2022.123725

