1. Tình hình ngành công nghiệp tôm tại Việt Nam
Ngành tôm là một trong những ngành kinh tế mũi nhọn, đóng vai trò quan trọng trong xuất khẩu thủy sản Việt Nam ra thế giới. Tuy nhiên, ngành nuôi tôm luôn phải đối mặt với những thách thức nghiêm trọng từ các bệnh dịch nguy hiểm như Đốm trắng (WSSV), Hoại tử Gan tụy Cấp tính (AHPND/EMS), Vi bào tử Enterocytozoon hepatopenaei (EHP) và Hội chứng Taura (TS)…. Những đợt bùng phát dịch bệnh này thường dẫn đến thiệt hại kinh tế lớn do tỷ lệ tử vong cao và năng suất giảm sút đáng kể. Vì vậy, việc chẩn đoán chính xác và kịp thời là yếu tố then chốt để đảm bảo năng suất và lợi nhuận.
Các phương pháp chẩn đoán truyền thống như quan sát lâm sàng, soi tươi, nuôi cấy và phân lập vi khuẩn đóng vai trò nhất định, nhưng chúng vẫn tồn tại những hạn chế đáng kể về độ nhạy, độ đặc hiệu và thời gian phản hồi kết quả. Quan sát lâm sàng dễ nhầm lẫn do triệu chứng không đặc trưng; trong khi soi tươi chỉ phát hiện được các mầm bệnh có kích thước lớn hoặc mật độ cao; nuôi cấy vi khuẩn lại mất nhiều thời gian, làm chậm trễ các quyết định phòng chống dịch. Trong bối cảnh đó, Real-time PCR (qPCR) nổi bật và vượt trội hơn hẳn so với các phương pháp còn lại trong chẩn đoán tôm bệnh.
Với độ nhạy cao cho phép phát hiện mầm bệnh ở nồng độ cực thấp trước khi xuất hiện triệu chứng lâm sàng; độ đặc hiệu cao khi chỉ phát hiện DNA/RNA của tác nhân gây bệnh giúp đảm bảo kết quả chính xác, tránh nhầm lẫn với các tác nhân gây bệnh khác, điều mà các phương pháp dựa trên triệu chứng hay hình thái thường khó đạt được; tốc độ trả kết quả nhanh chóng (khoảng 1-2 giờ) là yếu tố then chốt giúp đưa ra các quyết định quản lý dịch bệnh kịp thời, từ việc cách ly tôm bệnh, xử lý ao nuôi đến điều chỉnh quy trình sản xuất. Nhờ những ưu điểm vượt trội này, qPCR không chỉ là một công cụ chẩn đoán nhanh chóng, chính xác và hiệu quả mà còn là nền tảng vững chắc, giúp ngành tôm chuyển mình từ tư duy phòng chống dịch bệnh bị động sang chủ động sàng lọc, giám sát, đảm bảo sự phát triển bền vững trong tương lai.
2. Cách thu và bảo quản mẫu cho Real-time PCR
Chất lượng của kết quả chẩn đoán phụ thuộc trực tiếp vào chất lượng của mẫu ban đầu. Thu thập, xử lý và bảo quản mẫu đúng cách là rất quan trọng để giảm thiểu nhiễm chéo, ngăn chặn sự phân hủy của DNA/RNA và đảm bảo phát hiện chính xác tác nhân gây bệnh.
2.1. Nguyên tắc chung khi thu mẫu
- Đảm bảo an toàn sinh học: Sử dụng găng tay, khẩu trang, và khử trùng dụng cụ lấy mẫu trước và sau khi sử dụng để tránh lây nhiễm chéo, thao tác cẩn thận để tránh giọt bắn hoặc tiếp xúc không mong muốn với mẫu.
- Lấy mẫu đại diện: Mẫu phải thể hiện được tình trạng chung của ao nuôi hoặc của
- quần thể tôm.
- Ghi chép đầy đủ thông tin: Ghi lại ngày giờ lấy mẫu, vị trí lấy mẫu, đặc điểm tôm/nước/bùn, các dấu hiệu bất thường (nếu có) và thông tin về ao nuôi.
- Bảo quản mẫu: Mẫu được bảo quản ngay ở nhiệt độ từ 2°C đến 8°C và chuyển đến phòng thí nghiệm không quá 48h sau khi lấy mẫu hoặc bảo quản trong ethanol từ 96% đến 100%. Mẫu chuyển đến phòng thí nghiệm nếu chưa phân tích ngay phải được bảo quản ở nhiệt độ -20°C đến -80°C hoặc trong ethanol từ 96% đến 100%.
2.2. Quy trình thu và bảo quản mẫu
Mẫu tôm:
Lượng mẫu: Số lượng tôm trên mỗi mẫu phụ thuộc vào kích cỡ của tôm.
– Giai đoạn ấu trùng, hậu ấu trùng: 100mg
– Tôm trưởng thành, tôm bố mẹ: lấy từ 5 con/mẫu – 10 con/mẫu.
Vị trí lấy mẫu:
– Đối với ao có dấu hiệu bệnh: ưu tiên thu tôm có biểu hiện bệnh hoặc tôm ở các vị trí có tôm biểu hiện bất thường (ví dụ: bơi lờ đờ ở mép ao, dạt bờ, vỏ mềm, đổi màu, có đốm trắng, gan tụy nhạt màu/trắng đục, ruột rỗng, phân trắng, teo cơ…).
– Đối với ao kiểm tra định kỳ: (không có dấu hiệu bệnh rõ ràng hoặc kiểm): Lấy mẫu tôm ở nhiều vị trí khác nhau trong ao (ít nhất 5 điểm, ví dụ: bốn góc ao, giữa ao,…) để đảm bảo tính đại diện của quần thể tôm.
Bảo quản:
– Cho tôm vào túi sạch có chứa nước ao đối với tôm còn sống.
– Nếu tôm sắp chết, đã chết, hoặc xử lý mẫu tại chỗ, trong quá trình vận chuyển mẫu được bảo quản ở 2-8°C không quá 48 giờ hoặc bảo quản trong cồn 96% – 100%.
Mẫu bùn:
Lượng mẫu: Lấy khoảng 50-100 g mẫu bùn
Vị trí lấy mẫu: Lấy 5-10 g bùn bề mặt (2-5cm) ở các vị trí khác nhau trong ao (ít nhất 5 điểm, ví dụ: bốn góc ao, giữa ao, gần cống xả hoặc khu vực cho ăn…) để đảm bảo tính đại diện của ao tôm, lượng bùn gộp có thể lên đến 50-100 g.
Bảo quản: Trong quá trình vận chuyển, mẫu được bảo quản ở 2-8°C không quá 48 giờ.
Mẫu nước:
Lượng mẫu: Lấy khoảng 0,5-1 L mẫu nước
Vị trí lấy mẫu: Lấy ít nhất 0,5 L mẫu nước ao tầng đáy (cách 20-30 cm so với đáy ao) ở các vị trí khác nhau trong ao (ít nhất 5 điểm, ví dụ: bốn góc ao, giữa ao, tầng đáy và gần khu vực cho ăn…) để đảm bảo tính đại diện của ao tôm.
Bảo quản: Trong quá trình vận chuyển, mẫu được bảo quản ở 2-8°C không quá 48 giờ.
Mẫu phết bề mặt:
Lượng mẫu: Sử dụng 1 que phết mẫu cho một khu vực xác định (khoảng 10×10 cm), tùy thuộc vào diện tích bề mặt muốn kiểm tra mà sử dụng số que phết mẫu cho phù hợp (ví dụ: 1-2 mẫu cho dụng cụ, 3-5 mẫu cho bạt ao,…)
Vị trí lấy mẫu: Ưu tiên lấy mẫu ở các bề mặt tiếp xúc trực tiếp với tôm, thức ăn, nguồn nước như: khu vực cho ăn, bạt ao, dụng cụ
Bảo quản: Mẫu phết bề mặt phải được bảo quản trong dung dịch đệm PBS 1X hoặc nước muối sinh lý để thay thế. Trong quá trình vận chuyển, mẫu được bảo quản ở 2-8°C không quá 48 giờ.
Tách chiết DNA/RNA
Tùy thuộc vào loại mẫu (mẫu tôm: mô, mang, chân bơi, gan, tụy, đường ruột; mẫu nước; mẫu bùn; mẫu phết bề mặt) và tác nhân gây bệnh (DNA/RNA) mà sử dụng bộ kit tách chiết cho phù hợp. Lưu ý: tuân thủ hướng dẫn sử dụng của nhà sản xuất.
4. Đọc và phân tích kết quả Real-time PCR
4.1. Tầm quan trọng của các đối chứng trong real-time PCR
- Đối chứng âm tách chiết (Extraction Negative Control): là mẫu không chứa vật chất di truyền (DNA/RNA) được thực hiện toàn bộ quy trình tách chiết tương tự các mẫu thật nhằm kiểm tra quá trình tách chiết có bị nhiễm chéo hay không.
- Đối chứng âm (Negative Control): là mẫu không chứa trình tự gene mục tiêu trong hỗn hợp phản ứng qPCR, được sử dụng để đảm bảo độ đặc hiệu của mồi sử dụng và xác nhận kết quả chỉ khuếch đại trình tự gene mục tiêu. Nước siêu sạch không chứa DNAse và RNAse (nuclease-free water) được thêm vào hỗn hợp master mix nhằm kiểm tra xem hóa chất và thiết bị có bị ngoại nhiễm trong quá trình nạp mẫu hay từ sản phẩm khuếch đại trước đó hay không.
- Đối chứng dương (Positive Control): là một chất chuẩn (Standard) hoặc là mẫu axit nucleic có số lượng bản sao đã biết trước (Amplicon) giống với trình tự của DNA đích. Kết quả của đối chứng dương luôn dương tính để chứng minh sự hoạt động hiệu quả của PCR mix đang sử dụng, đảm bảo độ nhạy và đặc hiệu của cặp mồi, xác nhận nhiệt độ bắt cặp là chính xác, thời gian kéo dài đủ và không có chất ức chế PCR.
- Chứng nội (Internal Control – IC): là đoạn DNA/RNA được khuếch đại cùng với trình tự mục tiêu trong cùng một phản ứng real-time PCR hoặc trong cùng một lần chạy real-time PCR. Chứng nội thường dùng một đoạn gene không cạnh tranh với gene đích, được đưa vào quá trình tách chiết hoặc pha mix, mục đích để kiểm qua chất lượng phản ứng PCR, kiểm tra sự hiện diện của chất ức chế có trong mẫu.
4.2. Cách đọc kết quả Real-time PCR
Khi phân tích kết quả real-time PCR cần đọc kết hợp dữ liệu thô và dữ liệu phân tích là rất quan trọng để đảm bảo độ tin cậy và đánh giá chính xác kết quả, hạn chế các trường hợp âm tính giả, dương tính giả.
- Dữ liệu thô là dữ liệu gốc thu được trực tiếp từ máy real-time PCR trong quá trình chạy phản ứng, trước khi được phần mềm xử lý tự động.
- Dữ liệu phân tích là kết quả đã được phần mềm xử lý từ dữ liệu thô, cho ra các giá trị cụ thể dùng để đánh giá định tính hoặc định lượng.

Bước 1: Kiểm tra hệ thống đối chứng
- Chứng âm tách chiết phải cho kết quả âm tính, đảm bảo hóa chất tách chiết và quá trình thao tác tách chiết không bị ngoại nhiễm.
- Chứng âm PCR phải cho kết quả âm tính, đảm bảo độ đặc hiệu của phản ứng, hóa chất real-time PCR và thiết bị không bị ngoại nhiễm trong quá trình nạp mẫu, hay từ sản phẩm khuếch đại trước đó.
- Chứng dương phải cho kết quả dương tính, đảm bảo các thành phần trong phản ứng real-time PCR và thiết bị hoạt động bình thường.
- Chứng nội IC:
+ Thêm vào quá trình tách chiết: Chứng âm tách chiết và các mẫu phải cho kết quả dương tính với chứng nội. Từ đó kiểm tra quá trình tách chiết có thành công hay không, mẫu có chất ức chế phản ứng real-time PCR hay không.
+ Thêm vào quá trình nạp mẫu: Chứng âm và các mẫu phải cho kết quả dương tính với chứng nội. Từ đó kiểm tra mẫu có chất ức chế phản ứng real-time PCR hay không.
Bước 2: Thiết lập base line (đường nền)
Đường nền (Baseline): là đường biểu diễn mức độ tín hiệu trong suốt những chu kỳ đầu của real-time PCR. Việc thiết lập baseline là bước quan trọng trong phân tích kết quả real-time PCR do baseline không cố định, giá trị baseline sẽ ảnh hưởng nhiều đến kết quả cuối cùng. Nếu điều chỉnh giá trị baseline quá thấp, kết quả sẽ rất dễ thu nhận tín hiệu nhiễu (dương tính giả), ngược lại giá trị baseline quá cao, kết quả sẽ có độ chính xác thấp vì bỏ qua các mẫu dương yếu (âm tính giả). Vì vậy, baseline nên được điều chỉnh về khoảng 5% so với giá trị tín hiệu huỳnh quang chứng dương.
Bước 3: Phân tích kết quả
Sau khi điều chỉnh base line, tiến hành đọc kết quả, ghi nhận giá trị Ct và phân tích kết quả theo hướng dẫn sử dụng của bộ kit real-time được sử dụng.
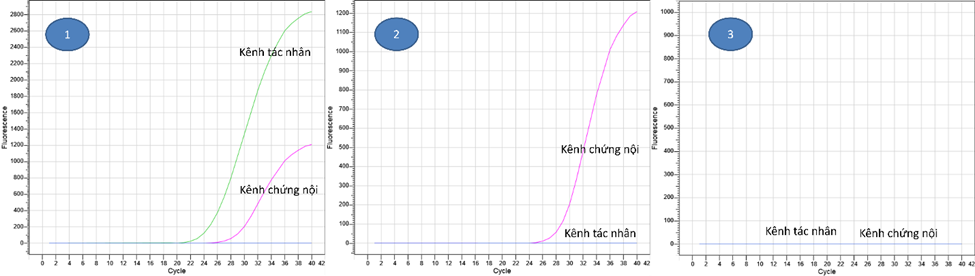
- Mẫu âm tính: là mẫu không có đường tín hiệu khuếch đại và không có giá trị Ct ở kênh tác nhân (No Ct: 0.00). Đối với mẫu âm tính, bắt buộc luôn xuất hiện đường tín hiệu khuếch đại ở kênh chứng nội.
- Mẫu Dương tính: là mẫu có đường tín hiệu khuếch đại và có giá trị Ct ở kênh tác nhân. Đối với mẫu dương tính, xuất hiện đường tín hiệu khuếch đại của cả kênh tác nhân và kênh chứng nội. Trong một số trường hợp giá trị Ct của kênh tác nhân lên sớm dẫn đến tín hiệu kênh chứng nội âm tính.
Theo TCVN, các mẫu dương tính có đường tín hiệu khuếch đại và giá trị Ct>35 ở kênh tác nhân được xem là mẫu nghi ngờ. Trong trường hợp này, cần thực hiện xét nghiệm lại một lần nữa bằng phản ứng real-time PCR hoặc bằng một phương pháp tương đương để khẳng định kết quả. - Không thể kết luận: Đường tín hiệu ở cả kênh tác nhân và kênh chứng nội đều âm tính. Trong trường hợp này, có thể mẫu đang tồn tại chất ức chế, cần pha loãng mẫu 10 lần để tiến hành xét nghiệm lại.
Theo TCVN, để kết luận mẫu tôm nhiễm bệnh khi có các đặc điểm dịch tễ, triệu chứng lâm sàng, bệnh tích đặc trưng của bệnh và có kết quả xét nghiệm dương tính bằng phương pháp real-time PCR hoặc phương pháp tương đương. Tuy nhiên, không phải lúc nào kết quả dương tính với phương pháp real-time PCR đều đi kèm với đặc điểm dịch tễ, triệu chứng lâm sàng hay bệnh tích đặt trưng của bệnh. Nhờ vào độ nhạy vượt trội, cho phép phát hiện mầm bệnh ngay cả khi chúng hiện diện ở nồng độ cực thấp trong giai đoạn ủ bệnh, trước khi xuất hiện các triệu chứng lâm sàng. Kết hợp với độ nhạy cao, thời gian trả kết quả nhanh chóng làm cho real-time PCR trở nên cực kỳ quan trọng để can thiệp sớm, đưa ra các quyết định quản lý dịch bệnh kịp thời giúp ngăn chặn dịch bệnh bùng phát. Do đó real-time PCR trở thành phương pháp giúp phát hiện sớm dịch bệnh ở tôm một cách chính xác, nhanh chóng và hiệu quả.
5. Tài liệu tham khảo
- Taura Syndrome Virus (TSV) | Shrimp Disease Information – JALA
- Enterocytozoon hepatopenaei infection, environmental characteristics, shrimp health status, and microorganisms abundance in intensive Pacific white shrimp farming – ResearchGate
- Verbruggen, Bas, et al. “Molecular mechanisms of white spot syndrome virus infection and perspectives on treatments.” Viruses 8.1 (2016): 23.
- Tiêu chuẩn quốc gia TCVN 8710-5:2023 về bệnh thuỷ sản – quy trình chẩn đoán – phần 5: hội chứng taura ở tôm.
- Tiêu chuẩn quốc gia TCVN 8710-12:2019 về Bệnh thủy sản – Quy trình chẩn đoán – Phần 12: Bệnh vi bào tử do Enterocytozoon hepatopenaei ở tôm.


